题目内容
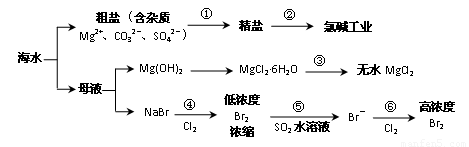
根据下图海水综合利用的工业流程图,判断下列说法正确的是( )

已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质
B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2
C.在过程④、⑥反应中每氧化0.2 mol Br- 需消耗2.24 L Cl2
D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
【答案】
D
【解析】
试题分析:A、过程①的提纯是发生了离子之间的反应有沉淀生成是化学过程,过程②通过氧化还原反应可产生2种单质分别是氯气和氢气,电解饱和食盐水的电解装置中,是将电能转化为化学能的装置,故A错误;B、因MgCl2•6H2O受热生成Mg(OH)Cl和HCl气体等,得不到无水MgCl2,若要由MgCl2•6H2O灼烧即可制得无水MgCl2,为防止Mg2+发生水解,应在HCl气氛中进行,故B错误; C、根据化学反应:2Br-+Cl2 =Br2 +2Cl-,可以知道每氧化0.2molBr-需消耗0.1molCl2,但没有说明是在标况下,故C错误确;D、因Br2+SO2 +2H2O=2HBr+H2SO4,反应后溶液呈酸性,能与金属容器反应,需解决其对金属设备的腐蚀问题,故D正确;故选D。
考点:本题考查了海水资源综合利用,涉及了离子的除杂、离子水解、氧化还原反应、元素及其化合物的有关知识进行综合利用,提高了试题的综合性,本题难度中等。

练习册系列答案
相关题目
根据下图海水综合利用的工业流程图,判断下列说法正确的是

已知:MgCl2?6H2O受热生成Mg(OH)Cl和HCl气体等.( )

已知:MgCl2?6H2O受热生成Mg(OH)Cl和HCl气体等.( )
| A、氯碱工业中电解饱和食盐水是一个将化学能转化为电能的过程 | B、在过程③中将MgCl2?6H2O灼烧即可制得无水MgCl2 | C、在过程④、⑥反应中每氧化0.2 mol Br- 需消耗0.1mol Cl2 | D、过程⑤在生产中无需解决其对金属设备的腐蚀问题 |