题目内容
16.下列说法符合事实的是( )| A. | SiO2溶于水成为硅酸 | |
| B. | CO2通入水玻璃中得到白色沉淀 | |
| C. | CO2通入饱和CaCl2溶液能生成白色沉淀 | |
| D. | 硅酸酸性比碳酸弱,所以SiO2不能跟Na2CO3反应 |
分析 A.二氧化硅不溶于水;
B.碳酸的酸性强于硅酸;
C.盐酸的酸性强于碳酸;
D.二氧化硅与碳酸钠反应生成硅酸钠和二氧化碳.
解答 解:A.二氧化硅不溶于水,不能与水反应生成硅酸,故A错误;
B.碳酸的酸性强于硅酸,CO2通入水玻璃反应生成碳酸钠和硅酸沉淀,故B正确;
C.CO2通入饱和CaCl2溶液不会发生反应,故C错误;
D.SiO2能跟Na2CO3反应生成硅酸钠和二氧化碳,故D错误;
故选B.
点评 本题考查了物质的性,题目难度不大,熟悉硅及其化合物的性质是解题关键,注意强酸制备弱酸的规律,侧重对基础知识的考查.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
6.完成下列实验所选择的装置和试剂不正确的是( )
| A | B | C | D | |
| 实验 | 配制 100mL 1mol/L NaCl溶液 | 提取碘水中的碘 | 制备氨气 | 除去二氧化碳中的氯化氢 |
装置 |  | 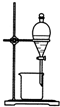 | 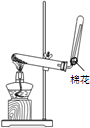 |  |
| 试剂 | NaCl固体、蒸馏水 | 碘水、CCl4 | NH4Cl和Ca(OH)2固体 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
7.下列叙述正确的是( )
| A. | 1mol任何气体的体积都是约22.4L | |
| B. | 标准状况下,氧气的体积约为22.4L | |
| C. | 标准状况下,1mol氢气、氮气的混合气体,体积约为22.4L | |
| D. | 标准状况下,18g水的体积恰好是22.4L |
4.恒容密闭的烧瓶里盛放气体M,在25℃时建立如下平衡:2M(g)?N(g),把烧瓶置于100℃的沸水中,在建立新平衡的过程中,烧瓶内混合气体的物理量始终不变的是( )
| A. | 平均相对分子质量 | B. | 密度 | ||
| C. | 容器内的压强 | D. | 物质的量 |
11.下列表示对应化学反应的离子方程式正确的是( )
| A. | MnO2与浓盐酸反应制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| B. | 醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O | |
| C. | Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
1.在10mL物质的量浓度为2mol•L-1的盐酸中加入0.65g锌片,它们恰好完全反应,生成氢气的体积为0.224L(标准状况下).请分析下面表格.
| 化学反应 | Zn+2HCl═ZnCl2+H2↑ | |||
| Zn | HCl | ZnCl2 | H2 | |
| 质量或气体体积 | 0.65g | 0.73gg | 1.36g | 0.224L |
| 物质的量 | ||||
| 物质的量之比 | ||||
| 微粒数 | ||||
| 结论:化学方程式中反应物或生成物化学式前的系数之比等于它们的 之比 | ||||
5.下列是除去括号内杂质的有关操作,其中正确的是( )
| A. | 氯化钠(氯化镁)-加硝酸银溶液,过滤 | |
| B. | 二氧化碳(氧气)-通过盛有石灰水的洗气瓶 | |
| C. | 二氧化碳(氯化氢)-让气体通过盛饱和Na0H溶液的洗气瓶 | |
| D. | 乙醇(乙酸)-加足量的Na0H溶液,蒸馏 |
6.将100mL 0.6mol/L的盐酸和等体积0.4mol/L的Ba(OH)2溶液混合后,所得混合液的体积为二者之和,则混合液中OH-离子物质的量浓度是( )
| A. | 0.4mol/L | B. | 0.2mol/L | C. | 0.1mol/L | D. | 0.05mol/L |
 现有21.6g由CO和CO2组成的混合气体,在标准状况下其体积为13.44L,回答下列问题:
现有21.6g由CO和CO2组成的混合气体,在标准状况下其体积为13.44L,回答下列问题: