题目内容
17.(1)在Fe(OH)3胶体中逐滴加入HI稀溶液,会出现一系列变化:①先出现红褐色沉淀,原因是:加入电解质,使胶体凝聚;
②随后沉淀溶解,溶液呈黄色,写出此过程反应的离子方程式:Fe(OH)3+3H+=Fe2++3H2O;
③最后溶液颜色加深,原因是:有I2生成,此过程的离子方程式是:2Fe3++2I-=2Fe2++I2;④如用稀盐酸代替HI稀溶液,能出现上述哪些相同的实验现象:①②(写序号).
(2)2.00gC2H2气体完全燃烧生成液态水和CO2气体,放出99.6kJ的热量,写出该反应燃烧的热化学反应方程式C2H2(g)+$\frac{5}{2}$O2(g)→2CO2(g)+H2O;△H=-1294.8kJ/mol.
分析 (1)①依据胶体聚沉的性质解答;
②氢氧化铁与氢碘酸发生酸碱中和反应;
③三价铁离子具有强的氧化性,能够氧化碘离子;
④Cl-比I-还原性弱,Cl-不能还原Fe3+,故导致现象不同.
(2)根据2.00g C2H2气体完全燃烧生成液态水和CO2,放出99.6kJ的热量,计算1molC2H2燃烧放出的热量,结合化学方程式书写热化学方程式.注意物质的聚集状态和反应热的单位等问题.
解答 解:(1)①碘化氢为可溶性电解质,能够使氢氧化铁胶体发生聚沉,出现红褐色沉淀;
故答案为:加入电解质,使胶体凝聚;
②氢氧化铁与氢碘酸发生酸碱中和反应:Fe(OH)3+3H+═Fe3++3H2O,所以沉淀溶解,溶液呈黄色;
故答案为:Fe(OH)3+3H+═Fe3++3H2O;
③三价铁离子具有强的氧化性,能够氧化碘离子,生成单质碘,反应的离子方程式为:2Fe3++2I-═I2+2Fe2+,所以最后溶液颜色加深;
故答案为:有I2生成;2Fe3++2I-═I2+2Fe2+;
④用稀盐酸代替稀HI溶液,Cl-比I-还原性弱,Cl-不能还原Fe3+,不会发生铁离子的还原反应,只会出现红褐色沉淀,随后沉淀溶解,溶液呈黄色的现象,故答案为:①②.
(2)C2H2气体完全燃烧反应的化学方程式为:2C2H2+5O2$\stackrel{加热}{→}$4CO2+2H2O,2.00g C2H2气体n(C2H2)=$\frac{2g}{26g/mol}$=$\frac{1}{13}$mol,放出99.6kJ的热量,则1molC2H2燃烧放出的热量为:99.6kJ×13=1294.8KJ,
则热化学方程式为:C2H2(g)+$\frac{5}{2}$O2(g)→2CO2(g)+H2O;△H=-1294.8kJ/mol,故答案为:C2H2(g)+$\frac{5}{2}$O2(g)→2CO2(g)+H2O;△H=-1294.8kJ/mol.
点评 本题考查氢氧化铁胶体的制备和性质、热化学方程式书写,以及相关化学方程式和离子方程式的书写,难度中等,了解胶体的制备及性质是解题关键.

| A. | 碳和一氧化碳 | B. | 1mol碳和2mol碳 | ||
| C. | 1mol乙炔和2mol碳 | D. | 淀粉和纤维素 |
①合金的性质与其组成金属的性质不完全相同
②火烧孔雀石[Cu2(OH)2CO3]也属于还原法
③金属冶炼的本质是金属阳离子得到电子变成金属原子
④工业上金属Mg、Al都是用电解熔融氯化物制得的
⑤越活泼的金属越难冶炼.
| A. | ①②③ | B. | 只有④ | C. | ④⑤ | D. | ②③④ |
| A. | 碱金属原子的最外层电子数都是1,次外层电子数都是8 | |
| B. | 将SO2通入滴有紫色石蕊试液的水中,溶液变成红色 | |
| C. | 白磷易溶于水,不能保存在水中 | |
| D. | 高性能通信材料光 导纤维的主要原料是单品硅 |
| A. | 11.7g | B. | 5.85g | C. | 8g | D. | 15.5g |
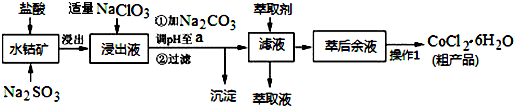
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)盐酸浸取水钴矿时为提高浸出率可采取的有效措施有研磨、搅拌、升温、适当增加酸的浓度、增加浸出时间(答一条即可),写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出该反应的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(2)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3.
(3)“操作1”中包含3个基本实验操作,依次是蒸发(浓缩)、冷却(结晶)和过滤.
(4)萃取剂对金属离子的萃取率与pH的关系如图.其使用的最佳pH范围是B.
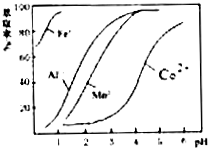
A.1.0~2.0 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
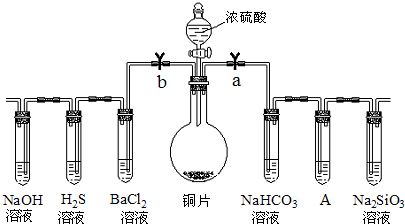
(1)验证碳、硅非金属性的相对强弱.(已知酸性:亚硫酸>碳酸)
①接仪器并检查装置气密性、加药品后,打开a关闭 b,然后滴入浓硫酸,加热.
②铜与浓硫酸反应的化学方程式是:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑.
装置A中的试剂可以是:品红溶液.
③能说明碳的非金属性比硅强的实验现象是:A中品红没有褪色,盛有Na2SiO3溶液的试管中出现白色沉淀.
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性.
①打开b,关闭a.
②H2S溶液中有浅黄色浑浊出现,化学方程式是:2H2S+SO2=3S↓+2H2O
③BaCl2溶液中无明显现象,将其分成两份,分別滴加下列溶液,将产生的沉淀的化学式填人下表相应位置:
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | BaSO4 | BaSO3 |
| A. | 自来水 | B. | 氯化钠溶液 | C. | 浓氢氧化钠溶液 | D. | 稀氨水 |