题目内容
氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过反应:
Al2O3+N2+3C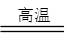 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮的化合价为+3
D.AlN的摩尔质量为41 g
【答案】
B
【解析】
试题分析:根据反应的化学方程式可知,氮气中氮元素的化合价从0价降低到-3价,得到3个电子。碳元素的化合价从0价升高到+2价,失去2个电子,所以氮气是氧化剂,碳是还原剂,A不正确,B正确;C不正确,AlN中氮的化合价为-3;D不正确AlN的摩尔质量为41g/mol,答案选B。
考点:考查氧化还原反应的有关判断、计算以及摩尔质量的有关计算
点评:该题是高考中的常见题型,属于中等难度的试题。氧化还原反应判断的关键是准确标出有关元素的化合价变化情况,然后根据有关的概念和要求逐一分析、判断即可。

练习册系列答案
相关题目
氮化铝广泛应用于电子陶瓷等工业领域.在一定条件下,AlN可通过反应:Al2O3+N2+3C
2AlN+3CO合成.下列叙述正确的是( )
| ||
| A、AlN的摩尔质量为41g |
| B、AlN中氮的化合价为+3 |
| C、每生成2mol AlN转移6mol电子 |
| D、反应中N2是还原剂,C是氧化剂 |
氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过反应:
Al2O3+N2+3C 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
| A.上述反应中,N2是还原剂,Al2O3是氧化剂 |
| B.上述反应中,每生成1 mol AlN需转移3 mol电子 |
| C.AlN中氮的化合价为+3 |
| D.AlN的摩尔质量为41 g |