题目内容
2.某烃X完全燃烧时生成等物质的量的CO2与H2O,1mol X需要消耗7.5mol O2,X能使溴的CCl4溶液褪色,则X结构(不考虑立体异构)最多有( )| A. | 5种 | B. | 3种 | C. | 7种 | D. | 4种 |
分析 1molX需要消耗7.5molO2且生成等物质的量的CO2与H2O,有机物中C原子个数与H原子个数的比值为1:2,即此有机物为CnH2n,且n+$\frac{2n}{4}$=7.5,则n=5,所以分子式为C5H10,该烃X能使溴的CCl4溶液褪色,说明含有1个碳碳双键,据此判断结构简式即可.
解答 解:1molX需要消耗7.5molO2且生成等物质的量的CO2与H2O,有机物中C原子个数与H原子个数的比值为1:2,即此有机物为CnH2n,且n+$\frac{2n}{4}$=7.5,则n=5,所以分子式为C5H10,该烃X能使溴的CCl4溶液褪色,说明含有1个碳碳双键,戊烯同分异构体为CH2=CH-CH2CH2CH3,CH3-CH=CH-CH2CH3,CH2=C(CH3)-CH2CH3,CH2=CH-CH(CH3)-CH3,CH3-CH=C(CH3)-CH3,X结构共5种,
故选A.
点评 本题主要考查的是有机物同分异构体的书写,依据产生二氧化碳与水的物质的量计算C、H个数比是解决本题的关键,题目难度不大.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案
相关题目
10.下列仪器名称为蒸馏烧瓶的是( )
| A. |  | B. |  | C. |  | D. |  |
11.为探究原电池的形成条件和反应原理,某同学设计了如下实验并记录了现象:
①向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
②向上述稀硫酸中插入铜片,没有看到有气泡生成;
③将锌片与铜片上端用导线连接,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快
④在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转.
下列关于以上实验设计及现象的分析,不正确的是( )
①向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
②向上述稀硫酸中插入铜片,没有看到有气泡生成;
③将锌片与铜片上端用导线连接,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快
④在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转.
下列关于以上实验设计及现象的分析,不正确的是( )
| A. | 实验①、②说明锌能与稀硫酸反应而铜不能 | |
| B. | 实验③说明发生原电池反应时会加快化学反应速率 | |
| C. | 实验③说明在该条件下铜可以与稀硫酸反应生成氢气 | |
| D. | 实验④说明该原电池中铜为正极、锌为负极,电子由锌沿导线流向铜 |
10.下列选项中有机物的同分异构体数目最多的是( )
| A. | 分子式为C5H10的烃 | B. | 分子式为C5H10O2的酯 | ||
| C. | 甲苯( )与氢气加成产物的一氯代物 )与氢气加成产物的一氯代物 | D. | 金刚烷(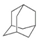 )的二氯代物 )的二氯代物 |
17.下列对某些离子的检验及结论一定正确的是( )
| A. | 加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,则原溶液中一定有SO42- | |
| B. | 加入碳酸钠溶液有白色沉淀生成,再加盐酸,沉淀消失,则原溶液中一定有Ba2+ | |
| C. | 向某稀溶液中加入Ba(NO3)2溶液后无明显现象,再滴入几滴硝酸酸化的AgNO3溶液,产生白色沉淀,说明一定是氯化物的溶液 | |
| D. | 加入NaOH溶液并加热,产生使湿润蓝色石蕊试纸变红的气体,则原溶液一定有NH4+ |
7.下列说法不正确的是( )
| A. | NH4Cl溶液呈酸性说明NH3•H2O是弱电解质 | |
| B. | CH3COONa溶液中c(Na+)>c(CH3COO-) | |
| C. | 常温下相同pH的NaOH溶液和CH3COONa溶液中水电离出的OH-浓度相同 | |
| D. | 常温下,在1 mol•L-1的盐酸溶液中加入等体积等浓度的氨水,溶液导电能力减弱 |
11.常温下,Ka (HCOOH)=1.77×10-4,Ka (CH3COOH)=1.75×10-5,Kb (NH3•H2O)=1.76×10-5,下列说法正确的是( )
| A. | 浓度均为0.1 mol•L-1的 HCOONa和NH4Cl 溶液中阳离子的物质的量浓度之和:前者小于后者 | |
| B. | 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等 | |
| C. | 0.2 mol•L-1 HCOOH 与 0.1 mol•L-1 NaOH 等体积混合后的溶液中:c(HCOO-)+c(OH-)=c(HCOOH)+c(H+) | |
| D. | 0.10 mol•L-1CH3COONa溶液中通入HCl至溶液呈中性:c(Na+)>c(Cl-)=c(CH3COOH) |
12.X、Y、Z、W 是原子序数依次增大的短周期主族元素.Y 与 W 同主族,Z 所在的族序数等于周期序数,X、Y 最外层电子数之和为 7;X、Z 原子的电子数总和与 Y、W原子的电子数总和之比为 7:12.下列说法正确的是( )
| A. | 元素 Y 的简单离子半径比 Z 的小 | |
| B. | 元素 Y 的简单气态氢化物的热稳定性比 W 的弱 | |
| C. | 由 X、Y 组成的物质与由 Y、W 组成的物质反应,反应类型可能为氧化还原反应 | |
| D. | 常温下,Z 的单质一定能溶于由 X、Y、W 三种元素组成的化合物的溶液 |
 一定温度下,在体积为2L的恒容密闭容器中充入1molN2和3molH2,一定条件下发生反应:N2(g)+3H2(g)?2NH3(g),测得其中N2物质的量随时间变化如图所示.回答下列问题:
一定温度下,在体积为2L的恒容密闭容器中充入1molN2和3molH2,一定条件下发生反应:N2(g)+3H2(g)?2NH3(g),测得其中N2物质的量随时间变化如图所示.回答下列问题: