��Ŀ����
18����27.2gCu��Cu2O�Ļ�����м���ijŨ�ȵ�ϡ����1.0L������������ȫ��Ӧ������NO ��Cu��NO3��2����������Һ�м���0.5mol/L ��NaOH��Һ2.0L����ʱ��Һ�����ԣ�������������ȫ��������������Ϊ39.2g�������й�˵������ȷ���ǣ�������| A�� | ��������ʵ���Ũ��Ϊ1.2mol/L | |
| B�� | ������NO�ڱ�״���µ����Ϊ3.36L | |
| C�� | Cu��Cu2O �����ʵ���֮��Ϊ1��2 | |
| D�� | ��Ӧ��ʣ��HNO3�����ʵ���Ϊ0.1mol |
���� ��������Һ�м���NaOH��Һ��ʱ��Һ�����ԣ�������������ȫ��������Һ������ΪNaNO3��n��NaNO3��=n��NaOH��=0.5mol/L��2.0L=1mol������ΪCu��OH��2������Ϊ39.2g�����ʵ���Ϊ$\frac{39.2g}{98g/mol}$=0.4mol������ͭԪ���غ���n��Cu��+2n��Cu2O��=n[Cu��OH��2]�����Է�Ӧ�����Һ��n[[Cu��NO3��2]=n[Cu��OH��2]=0.4mol��
A������NԪ���غ��֪ԭ������Һn��HNO3��=n��NO��+n��NaNO3��������NaԪ�ؿ�֪n��NaNO3��=n��NaOH�����ٸ���c=$\frac{n}{V}$���㣻
B����Cu��Cu2O�����ʵ����ֱ�Ϊxmol��ymol�����ݶ���������CuԪ�����ʵ����з��̼��㣬���õ���ת���غ����n��NO�����ٸ���V=nVm����NO�������
C������B�еļ�����н��
D������NԪ���غ㣬��֪nʣ����HNO3��+2n[[Cu��NO3��2]=n��NaNO3��������NaԪ�ؿ�֪n��NaNO3��=n��NaOH����
��� �⣺��������Һ�м���NaOH��Һ��ʱ��Һ�����ԣ�������������ȫ��������Һ������ΪNaNO3��n��NaNO3��=n��NaOH��=0.5mol/L��2.0L=1mol������ΪCu��OH��2������Ϊ39.2g�����ʵ���Ϊ$\frac{39.2g}{98g/mol}$=0.4mol������ͭԪ���غ���n��Cu��+2n��Cu2O��=n[Cu��OH��2]�����Է�Ӧ�����Һ��n[[Cu��NO3��2]=n[Cu��OH��2]=0.4mol��
��Cu��Cu2O�����ʵ����ֱ�Ϊxmol��ymol�����ݶ��������� 64x+144y=27.2������ͭԪ���غ���x+2y=0.4���������̽��x=0.2��y=0.1��
A������NԪ���غ��֪n��HNO3��=n��NO��+n��NaNO3��=0.2mol+1.0mol/L��1.0L=1.2mol������ԭ������Һ��Ũ��Ϊ$\frac{1.2mol}{1.0L}$=1.2mol/L����A��ȷ��
B�����ݵ���ת���غ��֪��3n��NO��=2n��Cu��+2n��Cu2O��������3n��NO��=2��0.2mol+2��0.1mol�����n��NO��=0.2mol�����Ա�״����NO�����Ϊ0.2mol��22.4L/mol=4.48L����B����
C��������������֪��n��Cu����n��Cu2O��=0.2mol��0.1mol=2��1����C����
D����Ӧ�����Һ�м�������������Һ����������������ͭ��Ӧ��ʣ����������������ᷴӦ�����Ϊ��������Һ�����ݵ�Ԫ���غ��֪��Ӧ����Һ��n��HNO3��+2n[[Cu��NO3��2]=n��NaNO3�������Է�Ӧ��ʣ����������ʵ���Ϊ��n��HNO3��=n��NaNO3��-2n[[Cu��NO3��2]=1mol-2��0.4mol=0.2mol����D����
��ѡA��
���� ���⿼�����ﷴӦ�ļ��㡢������ԭ��Ӧ�ļ��㣬��Ŀ�ѶȽϴ���ȷ������Ӧ��ʵ��Ϊ���ؼ���ע�������غ�˼���ڻ�ѧ�����е�Ӧ�÷�����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | 3�� | B�� | 4�� | C�� | 5�� | D�� | 6�� |
��
 ��
�� ��
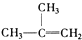
�� ��C2H4��CH2�TCH-CH�TCH2��C3H6
��C2H4��CH2�TCH-CH�TCH2��C3H6��
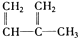 ��
��
| A�� | �ܺ͢� | B�� | �١��ں͢� | C�� | �ݺ͢� | D�� | �ܡ��͢� |
| A�� | XY2 | B�� | X3Y | C�� | X2 | D�� | Y2 |
������Һ ���ǽ��塡���ܲ��������ЧӦ����������ֽ���ݲ�������ֽ��
| A�� | �٢ܢ� | B�� | �ڢۢ� | C�� | �ڢۢ� | D�� | �٢ۢ� |
| A�� | 150mL 1mol/L�Ȼ�����Һ | B�� | 75mL 2mol/L�Ȼ�þ��Һ | ||
| C�� | 150mL 1.5mol/L�Ȼ�����Һ | D�� | 75mL 1mol/L�Ȼ�����Һ |
��101kPaʱ��2C��s��+O2��g���T2CO��g����H=-221kJ•mol-1
��ϡ��Һ�У�H+��aq��+OH-��aq���TH2O��l����H=-57.3kJ•mol-1
���н�����ȷ���ǣ�������
| A�� | ̼��ȼ���ȴ���110.5 kJ•mol-1 | |
| B�� | 2C��g��+O2��g���T2CO��g����H��-221 kJ•mol-1 | |
| C�� | 98%��Ũ������ϡ����������Һ��Ӧ����1molˮ���к���Ϊ-57.3kJ•mol-1 | |
| D�� | ϡ������ϡ����������Һ��Ӧ����1molˮʱ�ų�57.3kJ������ |
��2NO2��g��+NaCl��s���TNaNO3��s��+ClNO��g����H1��0 ƽ�ⳣ��K1
��2NO��g��+Cl2��g���T2ClNO��g����H2��0 ƽ�ⳣ��K2
10minʱ��Ӧ�ﵽƽ�⣬�����������ϵ��ѹǿ����20%��10min����ClNO��g����ʾ��ƽ����Ӧ����v��ClNO���T7.0��10-3mol•L•min-1��
����˵����ȷ���ǣ�������
| A�� | ��Ӧ4NO2��g��+2NaCl��s���T2NaNO3��s��+2NO��g��+Cl2��g����ƽ�ⳣ��$\frac{{{k}_{1}}^{2}}{{k}_{2}}$ | |
| B�� | ƽ���c��Cl2��=2.5��10-2mol•L-1 | |
| C�� | �����������ֲ��䣬��Ӧ�ں�ѹ�����½��У���ƽ�ⳣ��K2���� | |
| D�� | ƽ��ʱNO2��ת����Ϊ50% |
 ʵ���ҳ���MnO2��Ũ���ᷴӦ�Ʊ�Cl2������װ����ͼ��ʾ����
ʵ���ҳ���MnO2��Ũ���ᷴӦ�Ʊ�Cl2������װ����ͼ��ʾ����