题目内容
(16分)污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某化学研究小组利用软锰矿(主要成分为MnO2,另含有少量头铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已略去)。

请回答下列问题:
(1)上述流程脱硫实现了____(选填下列字母编号)。
A.废弃物的综合利用 B.白色污染的减少 C.酸雨的减少
(2)用MnCO3能除去溶液中Al3+和Fe3+,其原因是_____。
(3)已知:25℃、101kpa时,Mn(s)+O2(g)=MnO2(s) △H=-520kJ/mol
S(s)+O2(g)=SO2(g) △H=-297kJ/mol
Mn(s)+S(s)+2O2(g)=MnSO4(s) △H=-1065kJ/mol
SO2与MnO2反应生成无水MnSO4的热化学方程式是________________。
(4)MnO2可作超级电容器材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是
_ _。
(5)MnO2是碱性锌锰电池的正极材料。碱性锌锰电池放电时,正极的电极反应式是______。
(6)假设脱除的SO2只与软锰矿浆中的MnO2反应。按照图示流程,将a m3(标准状况)含SO2的体积分数为b%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量为c kg,则除去铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO2___________kg。

请回答下列问题:
(1)上述流程脱硫实现了____(选填下列字母编号)。
A.废弃物的综合利用 B.白色污染的减少 C.酸雨的减少
(2)用MnCO3能除去溶液中Al3+和Fe3+,其原因是_____。
(3)已知:25℃、101kpa时,Mn(s)+O2(g)=MnO2(s) △H=-520kJ/mol
S(s)+O2(g)=SO2(g) △H=-297kJ/mol
Mn(s)+S(s)+2O2(g)=MnSO4(s) △H=-1065kJ/mol
SO2与MnO2反应生成无水MnSO4的热化学方程式是________________。
(4)MnO2可作超级电容器材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是
_ _。
(5)MnO2是碱性锌锰电池的正极材料。碱性锌锰电池放电时,正极的电极反应式是______。
(6)假设脱除的SO2只与软锰矿浆中的MnO2反应。按照图示流程,将a m3(标准状况)含SO2的体积分数为b%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量为c kg,则除去铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO2___________kg。
(1)A、C (2)消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀
(3)MnO2(s)+SO2(g) =MnSO4(s) △H=-248kJ/mol
(4)Mn2++2H2O-2e-=MnO2+4H+ (5)MnO2+H2O+e-=MnO(OH)+OH-
(6)
(3)MnO2(s)+SO2(g) =MnSO4(s) △H=-248kJ/mol
(4)Mn2++2H2O-2e-=MnO2+4H+ (5)MnO2+H2O+e-=MnO(OH)+OH-
(6)

试题分析:(1)白色污染主要是塑料等难降解的物质形成的,SO2能形成酸雨,因此脱硫实现了废弃物的综合利用,同时也减少了酸雨形成,即答案选AC。
(2)由于碳酸锰能消耗溶液中的酸,降低溶液的酸性,从而促进Al3+和Fe3+水解生成氢氧化物沉淀。
(3)已知:热化学方程式①Mn(s)+O2(g)=MnO2(s) △H=-520kJ/mol,②S(s)+O2(g)=SO2(g)
△H=-297kJ/mol,③Mn(s)+S(s)+2O2(g)=MnSO4(s) △H=-1065kJ/mol,则根据盖斯定律可知③-(①+③)即得到SO2与MnO2反应生成无水MnSO4的热化学方程式MnO2(s)+SO2(g) =MnSO4(s) △H=-248kJ/mol。
(4)电解池中阳极失去电子发生氧化反应,则用惰性电极电解MnSO4溶液可制得MnO2,因此阳极是锰离子放电,其阳极电极反应式是Mn2++2H2O-2e-=MnO2+4H+。
(5)原电池中负极失去电子,正极得到电子,因此碱性锌锰电池放电时,正极是二氧化锰得到电子,则电极反应式是MnO2+H2O+e-=MnO(OH)+OH-。
(6)实际参加反应的SO2的物质的量是
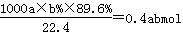 ,根据方程式MnO2(s)+SO2(g) =MnSO4(s)可知生成硫酸镁的物质的量是0.4abmol。最终生成二氧化锰是c kg,则根据方程式3MnSO4+2KMnO4+2H2O=5MnO2+K2SO4+2H2SO4可知,因此消耗硫酸锰的物质的量是
,根据方程式MnO2(s)+SO2(g) =MnSO4(s)可知生成硫酸镁的物质的量是0.4abmol。最终生成二氧化锰是c kg,则根据方程式3MnSO4+2KMnO4+2H2O=5MnO2+K2SO4+2H2SO4可知,因此消耗硫酸锰的物质的量是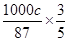 mol,则除去铁、铝、铜、镍等杂质时,所引入的锰元素的物质的量是
mol,则除去铁、铝、铜、镍等杂质时,所引入的锰元素的物质的量是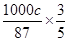 mol-0.4abmol,相当于二氧化锰的质量是(
mol-0.4abmol,相当于二氧化锰的质量是(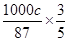 mol-0.4abmol)×87g/mol=(600c-34.8ab)g=
mol-0.4abmol)×87g/mol=(600c-34.8ab)g=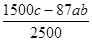 kg
kg
练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
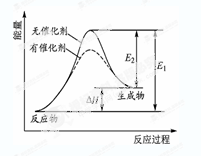
 Sn(白,s)ΔH3=+2.1 kJ·mol-1
Sn(白,s)ΔH3=+2.1 kJ·mol-1 H
H
 请在答题卡上写出并配平反应式(a);
请在答题卡上写出并配平反应式(a);


