题目内容
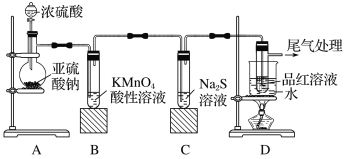
【题目】常温下,向1L0.1mol·L-1NH4Cl溶液中不断加入固体NaOH后,NH4+与NH3·H2O的变化趋势如右图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )

A. M点溶液中水的电离程度比原溶液小
B. 在M点时,n(OH-)-n(H+)=(a-0.05)mol
C. 随着NaOH的加入,![]() 不断增大
不断增大
D. 当n(NaOH)=0.05mo1时,溶液中有:c(Cl-)> c(NH4+)>c(Na+)>c(OH-)>c(H+)
【答案】C
【解析】
常温下,向1L0.1mol·L-1NH4Cl溶液中不断加入固体NaOH,则溶液中发生反应NH4++OH-=NH3H2O,随着反应进行,c(NH4+)不断减小,c(NH3H2O)不断增大。
A项、M点是向1L 0.1molL-1NH4Cl溶液中,不断加入NaOH固体后,反应得到氯化铵和一水合氨的混合溶液,溶液中铵根离子浓度和一水合氨浓度相同,一水合氨是一元弱碱抑制水电离,此时水的电离程度小于原氯化铵溶液中水的电离程度,故A正确;
B项、根据电荷守恒c(H+)+c(NH4+)+c(Na+)=c(OH-)+c(Cl-),可得n(OH-)-n(H+)=[c(NH4+)+c(Na+)-c(Cl-)]×1L,在M点时c(NH4+)=0.05molL1,c(Na+)=amolL1,c(Cl-)=0.1molL1,带入数据可得n(OH-)-n(H+)=[0.05molL-1+a molL-1-0.1molL-1]×1L=(a-0.05)mol,故B正确;
C项、氨水的电离常数Kb=![]() ,则
,则![]() =
=![]() ,温度不变Kb不变,随着NaOH的加入,c(NH4+)不断减小,
,温度不变Kb不变,随着NaOH的加入,c(NH4+)不断减小,![]() 不断减小,则
不断减小,则![]() 不断减小,故C错误;
不断减小,故C错误;
D项、当n(NaOH)=0.05mol时,NH4Cl和NaOH反应后溶液中溶质为等物质的量的NH3H2O和NH4Cl、NaCl,NH3.H2O的电离程度大于NH4Cl水解程度,导致溶液呈碱性,钠离子、氯离子不水解,所以溶液中离子浓度大小顺序是c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+),故D正确。
故选C。