题目内容
【题目】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2。为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO2转化为有用的产品。
治理方案Ⅰ:
(1)将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:_______________、_______________。
治理方案Ⅱ:
某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下流程既去除尾气中的SO2,又制得电池材料MnO2 (反应条件已省略)。
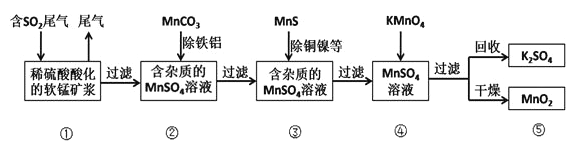
请回答下列问题:
(2)用MnCO3能除去溶液中Al3+和Fe3+其原因是___________________________,用MnS除去溶液中的Cu2+的离子方程式为_______________。
(3)流程图④过程中发生的主要反应的化学方程式为___________________。
(4)MnO2可作超级电容器材料。工业上用下图所示装置制备MnO2。接通电源后,A电极的电极反应式为:_______________,当制备lmol MnO2,则膜两侧电解液的质量变化差(△m左-△m右)为_______________g。

【答案】 2H2SO3+O2=2H2SO4 2(NH4)2SO3+O2=2(NH4)2SO4 2NH4HSO3+O2=2NH4HSO4(任填两个) 消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀 MnS(s)+Cu2+(aq)=CuS(s)+Mn2+(aq) 2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2 H2SO4 Mn2++2H2O-2e-=MnO2+4H+ 89
【解析】由流程可知,二氧化硫能与二氧化锰反应生成硫酸锰,用MnCO3调节溶液pH,使溶液中Al3+和Fe3+转化为沉淀,过滤除去,MnS将铜、镍离子还原为单质,过滤分离,滤液中加入高锰酸钾与硫酸锰反应生成二氧化锰,通过过滤获得二氧化锰。
(1)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2。将尾气通入氨水中,能发生多个反应,其中可能发生的氧化还原反应有2H2SO3+O2=2H2SO4、2(NH4)2SO3+O2=2(NH4)2SO4、2NH4HSO3+O2=2NH4HSO4,故答案为:2H2SO3+O2=2H2SO4、2(NH4)2SO3+O2=2(NH4)2SO4、2NH4HSO3+O2=2NH4HSO4(任填两个);
(2)用MnCO3能除去溶液中Al3+和Fe3+,其原因是:消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀,用MnS除去溶液中的Cu2+的离子方程式为:MnS(s)+Cu2+(aq)=CuS(s)+Mn2+(aq),故答案为:消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀;MnS(s)+Cu2+(aq)=CuS(s)+Mn2+(aq);
(3)高锰酸钾与硫酸锰反应生成二氧化锰,还生成硫酸钾,由元素守恒可知还生成硫酸,反应方程式为:2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2H2SO4,故答案为:2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2H2SO4;
(4)MnO2可作超级电容器材料.电解硫酸锰溶液制备MnO2,Mn元素发生氧化反应,由装置图可知,B电极上有气体生成,发生还原反应,应是氢离子放电生成氢气,A为阳极,阳极上是Mn2+失去电子得到MnO2,由电荷守恒可知还有H+生成,氢离子通过质子交换膜移向右室,阳极电极反应式为:Mn2++2H2O-2e-=MnO2+4H+,根据电子转移可知移向右室的氢离子生成氢气,右室电解质溶液质量不变,两侧电解液的质量变化差为二氧化锰与移向右室氢离子的质量,当制备1mol MnO2,转移电子为2mol,则移向右室的氢离子为2mol,则膜两侧电解液的质量变化差(△m左-△m右)为1mol×87g/mol+2mol×1g/mol=89g,故答案为:Mn2++2H2O-2e-=MnO2+4H+;89。

 阅读快车系列答案
阅读快车系列答案