��Ŀ����
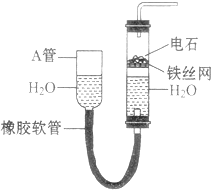
����Ŀ��������ʵ������ȡ������������ͭ��ʵ�飬����ʵ�鲽�裬�ش��й����⣮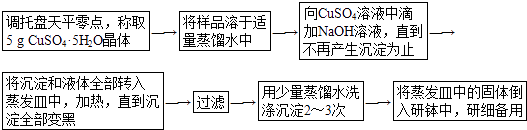
��1��������ƽ���ʱ����ָ��ƫ���ұߣ�Ӧ����ߵ���˿����������ҡ���������
��2���ܽ���ƷʱҪ�õ����������������� ��
��3����Ӧ���ɳ��������ӷ���ʽΪ ��
��4����������������Ҫ�õ����������������� ��
��5��������Ҫ�õ����������������� ��
��6��ϴ�ӳ�����Ŀ������ϴ�ӳ����ķ�������Ϊ�˼�������Ƿ�ϴ�Ӹɾ���Ӧ�����һ�ε�ϴ��Һ�м�����Һ��
��7������CuSO4��Һ�еμ��� 100mL NaOH��Һ����NaOH��Һ�����ʵ���Ũ������Ϊ ��
���𰸡�
��1������
��2�����裬���ٹ������ʵ��ܽ�
��3��Cu2++2OH���TCu��OH��2��
��4�����裬��ֹ��ֲ���������Һ�����ʷɽ�
��5������
��6����ȥ�����м��ӵĿ��������ʣ���������м�������ˮ��û�������ȴ�ˮ��Ȼ�������ظ�����2��3�Σ�BaCl2
��7��0.4mol/L
���������⣺��1����ָ��ƫ���ұߣ�˵���ұ��أ�����ᣬӦ����ߵ���˿�������������Դ��ǣ����ң���2���ܽ���ƷʱҪ�õ����������������ǣ����裬���ٹ������ʵ��ܽ⣬���Դ��ǣ����裬���ٹ������ʵ��ܽ⣻��3������ͭ���������Ʒ�Ӧ����������ͭ�������ƣ����ӷ���ʽΪ��Cu2++2OH���TCu��OH��2�������Դ��ǣ�Cu2++2OH���TCu��OH��2������4����������������Ҫ�õ����������������ǣ����裬��ֹ��ֲ���������Һ�����ʷɽ������Դ��ǣ����裬��ֹ��ֲ���������Һ�����ʷɽ�����5��������Ҫ�õ����������������ǣ����������Դ��ǣ���������6��ϴ�ӳ�����Ŀ���ǣ���ȥ�����м��ӵĿ��������ʣ�ϴ�ӳ����ķ����ǣ���������м�������ˮ��û�������ȴ�ˮ��Ȼ�������ظ�����2��3�Σ�Ϊ�˼�������Ƿ�ϴ�Ӹɾ���Ӧ�����һ�ε�ϴ��Һ�м���BaCl2��Һ�����Դ��ǣ���ȥ�����м��ӵĿ��������ʣ���������м�������ˮ��û�������ȴ�ˮ��Ȼ�������ظ�����2��3�Σ�BaCl2����7������ͭ��������ʵ���Ϊ ![]() =0.02mol����CuSO4Ϊ0.02mol����CuSO4+2NaOH=Cu��OH��2��+Na2SO4��֪����ҪNaOH���ʵ���Ϊ0.02mol��2=0.04mol����NaOH��Һ�����ʵ���Ũ������Ϊ
=0.02mol����CuSO4Ϊ0.02mol����CuSO4+2NaOH=Cu��OH��2��+Na2SO4��֪����ҪNaOH���ʵ���Ϊ0.02mol��2=0.04mol����NaOH��Һ�����ʵ���Ũ������Ϊ ![]() =0.4mol/L�����Դ��ǣ�0.4mol/L��
=0.4mol/L�����Դ��ǣ�0.4mol/L��

 ��ս100��Ԫ����Ծ�ϵ�д�
��ս100��Ԫ����Ծ�ϵ�д�