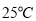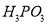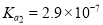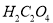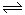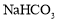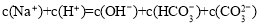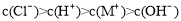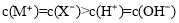��Ŀ����
�����й�������ȷ���� �� ��
A����Ũ�ȵ�NaClO��NaHCO3�����Һ�У�c��HClO��+c��ClO����= c��HCO ��+c��H2CO3��
��+c��H2CO3��
B��pH��4.5������֭��c��H+����pH=6.5�ķ���֭��c��H+����100��
C��100 ml pH��3��HA��Һ��HB��Һ�ֱ���������п��Ӧ��HA��Һ�ų��������϶࣬˵��HA�����Ա�HB��ǿ
D��pH=5.5��CH3COOH��CH3COONa�����Һ�У�c��Na+��> c��CH3COO����
B
��������
���������A������Ԫ���غ���ɣ�Ӧ��c��HClO��+c��ClO����= c��HCO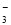 ��+c��H2CO3��+ c��CO32-��������B��pH��4.5������֭��c��H+��=1��10-4.5mol/L��pH=6.5�ķ���֭��c��H+��=1��10-6.5mol/L��ǰ���Ǻ��ߵ�100������ȷ��C��HA��Һ��HB��Һ�������ȣ�������Ũ����ȣ�������п��Ӧ����������HA�࣬˵����HA��Ũ�ȱ���HB��Ũ�ȴ�������������D��CH3COOH��CH3COONa�����Һ��pH=5.5��˵���������̶ȴ��ڴ��������ˮ��̶ȣ�����c��Na+��<c��CH3COO����������ѡB��
��+c��H2CO3��+ c��CO32-��������B��pH��4.5������֭��c��H+��=1��10-4.5mol/L��pH=6.5�ķ���֭��c��H+��=1��10-6.5mol/L��ǰ���Ǻ��ߵ�100������ȷ��C��HA��Һ��HB��Һ�������ȣ�������Ũ����ȣ�������п��Ӧ����������HA�࣬˵����HA��Ũ�ȱ���HB��Ũ�ȴ�������������D��CH3COOH��CH3COONa�����Һ��pH=5.5��˵���������̶ȴ��ڴ��������ˮ��̶ȣ�����c��Na+��<c��CH3COO����������ѡB��
���㣺������Һ���غ���ɵ�Ӧ�ã�pH�ļ��㣬����ǿ�����жϣ�����Ũ�ȵıȽ�

 �����ÿ�ʱѵ��ϵ�д�
�����ÿ�ʱѵ��ϵ�д� ��Ԫȫ��������ϵ�д�
��Ԫȫ��������ϵ�д� �»ƸԱ����ܾ�ϵ�д�
�»ƸԱ����ܾ�ϵ�д�����ѪҺ�д���ƽ�⣺CO2 + H2O  H2CO3
H2CO3  HCO3�� ��ʹѪҺpH������7.35~7.45֮�䣬����ͻᷢ�����ж�����ж�����֪pH��c(HCO3��)�Uc(H2CO3) �仯��ϵ���±���ʾ��������˵��������ȷ����
HCO3�� ��ʹѪҺpH������7.35~7.45֮�䣬����ͻᷢ�����ж�����ж�����֪pH��c(HCO3��)�Uc(H2CO3) �仯��ϵ���±���ʾ��������˵��������ȷ����
c(HCO3��)��c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
pH | 6.10 | 7.35 | 7.40 | 7.45 |
A��pH=7��ѪҺ�У�c(HCO3��) > c(H2CO3)
B�����巢�����ж�ʱ���ɾ�����עһ��Ũ�ȵ�NaHCO3��Һ�ⶾ
C�������½�pH=7.40��ѪҺϡ����pH=7ʱ��c(H+)��c(OH��)һ������
D��c(HCO3��)�Uc(H2CO3)=1ʱ��H2CO3�ĵ���̶�С��HCO3����ˮ��̶�

��15�֣��״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ����Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�����±���ʾ��
��ѧ��Ӧ | ƽ�ⳣ�� | �¶��� | |
500 | 800 | ||
��2H2��g��+CO��g�� | K1 | 2.5 | 0.15 |
��H2��g��+CO2��g�� | K2 | 1.0 | 2.50 |
��3H2��g��+CO2��g�� | K3 |
|
|
��1����Ӧ���� ������ȡ����ȡ�����Ӧ��
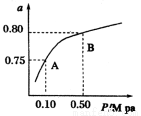
��2��ij�¶��·�Ӧ����H2��ƽ��ת���ʣ�a������ϵ��ѹǿ��P���Ĺ�ϵ����ͼ��ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K��A�� K��B�����>������<�����������ݷ�Ӧ���������Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3�� ����K1��K2��ʾ����
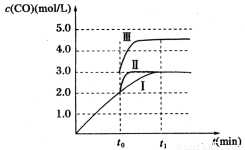
��3����3 L�ݻ��ɱ���ܱ������з�����Ӧ������֪c��CO���뷴Ӧʱ��t�仯��������ͼ��ʾ������t0ʱ�̷ֱ�ı�һ����������������Ϊ����������������
����������Ϊ������ʱ���ı�������� ��
����������Ϊ������ʱ���ı�������� ��
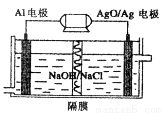
��4���״�ȼ�ϵ�����Ź㷺����;��ͬʱAl��AgO�����Ӧ�ù㷺������ �أ���ԭ �� ����ͼ��ʾ���õ�صĸ�����Ӧʽ�� ��
��5��һ�������¼״���һ����̼��Ӧ���Ժϳ����ᡣͨ��״���£���a mol/L�Ĵ�����b mol/L Ba��OH��2��Һ�������ϣ���Ӧƽ��ʱ��2c��Ba2+��=c��CH3COO�������ú�a��b�Ĵ���ʽ��ʾ�û����Һ�д���ĵ��볣��Ϊ ��