题目内容
(9分)氢气是工业上重要的原料。
(1)氢气用于工业合成氨 N2(g) + 3H2(g) 2NH3(g);ΔH =" -92.2" kJ·mol-1。
2NH3(g);ΔH =" -92.2" kJ·mol-1。
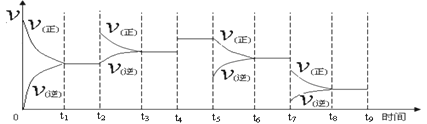
①一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t2 ﹑t4 ﹑t5﹑t7时刻所对应的实验条件改变分别是
t2 t4 t5 t7 。
②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为 。
(2)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入1mol及2mol碘化氢待反应:2HI(g)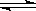 H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
(1)氢气用于工业合成氨 N2(g) + 3H2(g)
 2NH3(g);ΔH =" -92.2" kJ·mol-1。
2NH3(g);ΔH =" -92.2" kJ·mol-1。①一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t2 ﹑t4 ﹑t5﹑t7时刻所对应的实验条件改变分别是
t2 t4 t5 t7 。

②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为 。
(2)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入1mol及2mol碘化氢待反应:2HI(g)
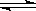 H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)(9分)(1)①t2增大N2或H2的浓度t4 加入催化剂
t5 减小NH3浓度 t7 降温 ② 4.0 (2分)
(2) < ; = ; = (其余1分1空)
t5 减小NH3浓度 t7 降温 ② 4.0 (2分)
(2) < ; = ; = (其余1分1空)
(1)①t2时刻正反应速率增大,逆反应速率不变,说明是增大了反应物的浓度;t4时正逆速率等倍数增大,说明了是加了催化剂;同理,t5是减少了产物浓度所致;t7时,正逆速率都减小,且相对正反应速率大,说明正向移动,应该是降低温度所致。
②N2(g) + 3H2(g) 2NH3(g);ΔH =" -92.2" kJ·mol-1
2NH3(g);ΔH =" -92.2" kJ·mol-1
0.5a 1.5a a -46.21kJ
可知:a=1,
N2(g) + 3H2(g) 2NH3(g)
2NH3(g)
初始n: 1 2 0
△n: 0.5 1.5 1
平衡n: 0.5 0.5 1
由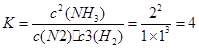
(2)可用下图来示意
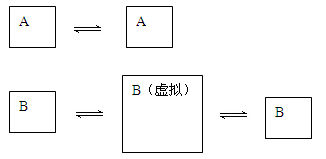
初始态 平衡
可把B的容积扩大一倍,虚拟出一个B的平衡状态,它应该与A的平衡状态相比:除了体积大一倍以外,其它诸如各物质的量浓度、转化率完全符合,再把这个虚拟出的状态压缩到最终态,由于平衡两边的气体系数和相等,故平衡不移动,但各物质浓度应该是A平衡状态的两倍。
②N2(g) + 3H2(g)
 2NH3(g);ΔH =" -92.2" kJ·mol-1
2NH3(g);ΔH =" -92.2" kJ·mol-10.5a 1.5a a -46.21kJ
可知:a=1,
N2(g) + 3H2(g)
 2NH3(g)
2NH3(g)初始n: 1 2 0
△n: 0.5 1.5 1
平衡n: 0.5 0.5 1
由
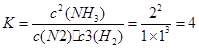
(2)可用下图来示意

初始态 平衡
可把B的容积扩大一倍,虚拟出一个B的平衡状态,它应该与A的平衡状态相比:除了体积大一倍以外,其它诸如各物质的量浓度、转化率完全符合,再把这个虚拟出的状态压缩到最终态,由于平衡两边的气体系数和相等,故平衡不移动,但各物质浓度应该是A平衡状态的两倍。

练习册系列答案
相关题目
 2HBr(g)。达到平衡状态后,下列说法中一定正确的是 ;能说明此反应达到平衡状态的是 。
2HBr(g)。达到平衡状态后,下列说法中一定正确的是 ;能说明此反应达到平衡状态的是 。 2Z(g) 此反应达到平衡的标志是( )
2Z(g) 此反应达到平衡的标志是( )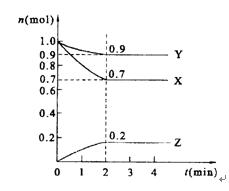
 [CuCl4]2-(绿)+4H2O能使黄绿色CuCl2溶液向蓝色转化的操作是
[CuCl4]2-(绿)+4H2O能使黄绿色CuCl2溶液向蓝色转化的操作是 2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是
2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是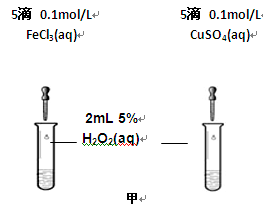
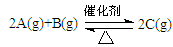 过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:
过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表: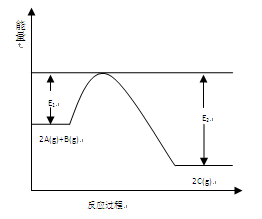
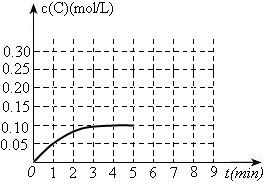
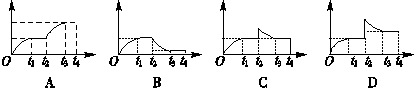
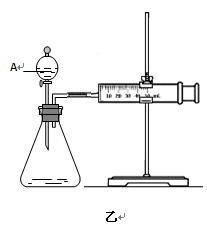
 ?2NH3在t1时刻达到平衡;t2时刻再从A口快速充入一定量NH3,封闭A;t3时刻重新达到平衡至t4。在0→t4时间内混合气中NH3的体积分数(纵坐标)随时间(横坐标)变化的曲线正确的是( )
?2NH3在t1时刻达到平衡;t2时刻再从A口快速充入一定量NH3,封闭A;t3时刻重新达到平衡至t4。在0→t4时间内混合气中NH3的体积分数(纵坐标)随时间(横坐标)变化的曲线正确的是( )