题目内容
【题目】科学家预言自然界中可能存在原子序数为114号的稳定同位素![]() X,根据原子结构理论和元素周期律下列预测错误的是
X,根据原子结构理论和元素周期律下列预测错误的是
A.![]() X位于第七周期,第ⅣA 族B.X是金属元素
X位于第七周期,第ⅣA 族B.X是金属元素
C.XO2是酸性氧化物D.X元素的化合价有+2和+4
【答案】C
【解析】
114号元素核外有7个电子层,且最外层电子数为4,由此进行分析判断。
A. 114号元素核外有7个电子层,且最外层电子数为4,因此在周期表中位于第七周期第IVA族,A项正确,不符合题意;
B. 第IVA族锗之后的元素均为金属元素,B项正确,不符合题意;
C. 同主族从上到下,最高价氧化物对应的水化物酸性逐渐减弱,碳酸为弱酸,因此114号元素最高价氧化物对应的水化物酸性可能不具有酸性,因此XO2可能为碱性氧化物,C项错误,符合题意;
D. 同主族的碳有+2和+4两种价态,那么114号元素也可能有+2和+4两种价态,D项正确,不符合题意;
答案选C。

 阅读快车系列答案
阅读快车系列答案【题目】以石墨为电极分别电解水和饱和食盐水,关于两个电解池反应的说法正确的是( )
A.阳极反应式相同
B.电解结束后所得液体的pH相同
C.阴极反应式相同
D.通过相同电量时生成的气体总体积相等(同温同压)
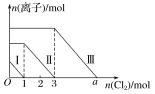
【题目】溴是一种重的化工原料,从淡化海水中提取溴的工艺流程如下:
![]()
⑴操作Ⅱ中,用饱和Na2CO3碱性溶液吸收Br2,过程中有CO2产生,反应的粒子方程式为______,当0.6 mol Br2被吸收时,转移电子的数目为______
![]() 步骤Ⅳ包含萃取,分液和蒸馏,该过程中不必用到的仪器有______
步骤Ⅳ包含萃取,分液和蒸馏,该过程中不必用到的仪器有______![]() 填序号
填序号![]()
a.烧杯 b.分液漏斗c.普通漏斗 d.玻璃棒 e.蒸发皿 f.冷凝管
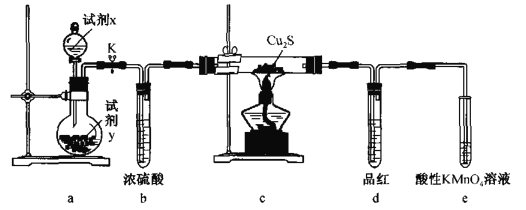
![]() 某化学兴趣小组利用高锰酸钾和浓盐酸反应制取氯气,并探究氯水的性质
某化学兴趣小组利用高锰酸钾和浓盐酸反应制取氯气,并探究氯水的性质
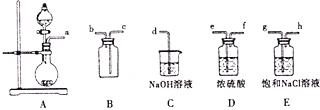
①将A,B,C相连,制得Cl2后加入适量水,即可制得氯水,将所得氯水分为两份,进行甲,乙两个实验,实验操作如下,将现象填入下表:
实验序号 | 实验操作 | 现象 |
甲 | 将氯水滴入品红溶液 | ______ |
乙 | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 |
②由实验乙不能推出氯气与水反应的产物具有酸性,原因是______,若要制备纯净干燥的Cl2,按气流方向连接各仪器接口,顺序为a→_____→_____→_____→_____→_____→_____→d
![]() 实验完毕后,假设装置C中氢氧化钠和
实验完毕后,假设装置C中氢氧化钠和![]() 恰好完全反应,其反应方程式为______,反应后溶液中离子浓度由大到小的顺序为______,常温下HClO的电离平衡常数为K,则常温下NaClO水解反应的平衡常数为______(用含Ka和Kw的表达式表示)
恰好完全反应,其反应方程式为______,反应后溶液中离子浓度由大到小的顺序为______,常温下HClO的电离平衡常数为K,则常温下NaClO水解反应的平衡常数为______(用含Ka和Kw的表达式表示)