题目内容
【题目】已知反应4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。
(1)在该反应中氧化剂是___,还原剂是___,1摩尔氧气完全参与反应,转移电子数目___。
(2)用双线桥标出该反应的电子转移方向及数目_____________,4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。
(3)该反应中氧化剂与氧化产物的氧化性由强到弱的关系是__________。
(4)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3 + C+S = K2S + 2NO2↑ + CO2↑。其中被还原的元素是____,被氧化的元素是____,氧化剂是___,还原剂是____,氧化产物是____,还原产物是_______ 。
【答案】O2 Fe(OH)3 4NA 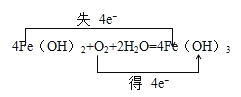 O2 > Fe(OH)3 N、S C KNO3、S C CO2 K2S、NO2
O2 > Fe(OH)3 N、S C KNO3、S C CO2 K2S、NO2
【解析】
反应中还原剂,被氧化,化合价升高,生成的产物为氧化产物;氧化剂,被还原,化合价降低,生成的产物为还原产物。
(1)该反应中,O2的化合价由0价变为-2价,得电子作氧化剂; Fe(OH)2中Fe的化合价由+2变为+3,失电子,作还原剂;1摩尔氧气完全参与反应,转移4mol电子,即4NA;
(2)用双线桥法表示为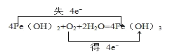 ;
;
(3)氧化性:氧化剂>氧化产物,则O2 > Fe(OH)3;
(4)反应中C作还原剂,被氧化,化合价升高,生成的产物为氧化产物;S、KNO3作氧化剂,被还原,化合价降低,生成的产物为还原产物;被还原的元素是N、S;被氧化的元素是C ;氧化产物是CO2;还原产物是K2S、NO2。

【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:

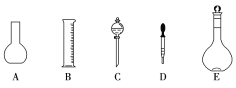
(1)仪器a的名称为____,仪器b中可选择的试剂为____。
(2)实验室中,利用装置A,还可制取的无色气体是____(填字母)。
A.Cl2 | B.O2 | C.CO2 | D.NO2 |
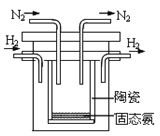
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体产生,上述现象证明NH3具有____性,写出相应的化学方程式:_______________________。
(4)E装置中浓硫酸的作用是_____________________________________。
(5)读取气体体积前,应对装置F进行的操作:____________________________。
(6)实验完毕,若测得干燥管D增重m g,装置F测得气体的体积为n L(已折算成标准状况),则氨分子中氮、氢的原子个数比为____(用含m、n字母的代数式表示)。