题目内容
(共计12分)
A.锌是一种重要的金属,锌及其化合物有着广泛的应用。
(1)葡萄糖酸锌[CH2OH(CHOH4COO)2Zn是目前市场上流行的补锌剂。写出Zn2+基
态电子排布式 ;葡萄糖[CH2OH(CHOH)4CHO]分子中碳原子杂化方式是 。
(2)Zn2+也能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子空间构型为 ;
在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在下图中
表示[Zn(NH3)4]2+中Zn2+与N之间的化学键 。
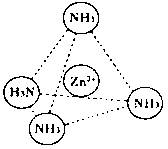
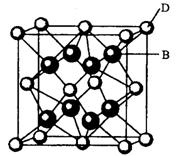
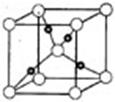
(3)下图表示锌与某种元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为 ;

该化合物的晶体熔点比干冰高得多,原因是 。
A.锌是一种重要的金属,锌及其化合物有着广泛的应用。
(1)葡萄糖酸锌[CH2OH(CHOH4COO)2Zn是目前市场上流行的补锌剂。写出Zn2+基
态电子排布式 ;葡萄糖[CH2OH(CHOH)4CHO]分子中碳原子杂化方式是 。
(2)Zn2+也能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子空间构型为 ;
在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在下图中
表示[Zn(NH3)4]2+中Zn2+与N之间的化学键 。

(3)下图表示锌与某种元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为 ;

该化合物的晶体熔点比干冰高得多,原因是 。
A(12分)
(1)1s22s22p63s23p63d10 (2分)
sp2、sp3(2分)
(2)三角锥形(2分)
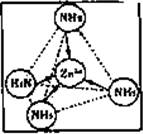 阶段(3分)
阶段(3分)
(3)ZnX 该化合物是原子晶体,而干冰是分子晶体。(3分)
(1)1s22s22p63s23p63d10 (2分)
sp2、sp3(2分)
(2)三角锥形(2分)
 阶段(3分)
阶段(3分)(3)ZnX 该化合物是原子晶体,而干冰是分子晶体。(3分)
略

练习册系列答案
相关题目
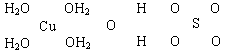
 ,试判断CA3溶于水后,形成CA3·H2O的合理结构 (填字母代号),推理依据是:
,试判断CA3溶于水后,形成CA3·H2O的合理结构 (填字母代号),推理依据是: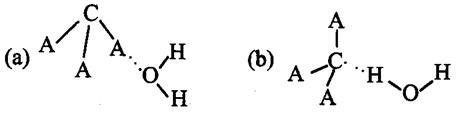
 性键
性键
 同特征:方向性和饱和性
同特征:方向性和饱和性 性键的分子都是极性分子
性键的分子都是极性分子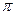 键数目为 。
键数目为 。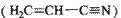 。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。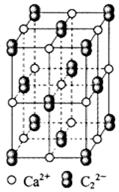
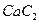 与水反应生成乙炔。
与水反应生成乙炔。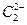 与
与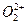 互为等电子体,
互为等电子体,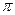 键数目为 。
键数目为 。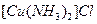 溶液生成
溶液生成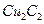 红棕色沉淀。
红棕色沉淀。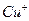 基态核外电子排布式为 。
基态核外电子排布式为 。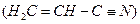 。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
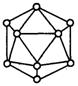
。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。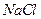 晶体相似(如图所示),但
晶体相似(如图所示),但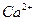 周围距离最近的
周围距离最近的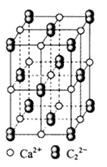
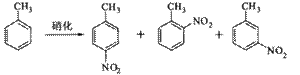
 溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。 NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为 。
NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为 。