题目内容
【题目】A、B、C、D、E五种物质中均含有同一种非金属元素,他们能发生如图所示的转化关系。若该元素用R表示,则A为R的氧化物,D与NaOH溶液反应生成C和H2。
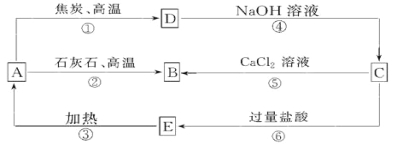
请回答:
(1)写出对应物质的化学式:A__________; C__________; E__________。
(2)反应①的化学方程式为: 。
(3)反应④的离子方程式为: 。
(4)H2CO3的酸性强于E的,请用离子方程式予以证明: _________________________。
【答案】(1)(3分)SiO2 Na2SiO3 H2SiO3(或H4SiO4)
(2)(2分)SiO2+2C![]() Si+2CO↑
Si+2CO↑
(3)(2分)Si+2OH-+H2O=== SiO32-+2H2↑
(4)(2分)SiO32-+CO2+H2O===H2SiO3↓+HCO32-
或SiO32-+CO2+H2O===H2SiO3↓+CO32- (写成H4SiO4同样给分)
【解析】
试题分析:非金属单质R能与NaOH溶液反应生成盐(Na2RO3)和氢气,则R为Si元素,由转化关系可知D为Si,A为SiO2,B为CaSiO3,C为Na2SiO3,E为H2SiO3,
(1)由以上分析可知A为SiO2,C为Na2SiO3,故答案为:SiO2;Na2SiO3;
(2)反应①的化学方程式为2C+SiO2![]() Si+2CO↑;
Si+2CO↑;
(3)反应④的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑;
(4)H2CO3的酸性强于H2SiO3的酸性,可在硅酸钠溶液中通入二氧化碳,如生成硅酸沉淀,可说明,反应的离子方程式为SiO32-+CO2+H2O=H2SiO3↓+CO32-。

练习册系列答案
相关题目