题目内容
NA表示阿伏伽德罗常数,下列叙述正确的是
| A.1 mol Cu和足量浓硝酸反应可收集NO2的分子数为2 NA |
| B.4℃时,3.6 mL 水所含的电子数为2 NA |
| C.30.8 g熟石膏(2CaSO4·H2O)中的钙离子数目为0.20 NA |
| D.200 mL 0.5 mol·L-1的Na2CO3溶液中阴离子数目小于0.1 NA |
B
解析试题分析:A、部分NO2转化为N2O4,错误;B、4℃时水的密度为1g/mg,3.6g水所含的电子数为2 NA,正确;C、熟石膏(2CaSO4·H2O)的摩尔质量为290g/mol,错误;D、碳酸根离子水解导致阴离子数目增多,错误。
考点:考查阿伏伽德罗常数有关问题。

练习册系列答案
相关题目
标准状况下,VL氯化氢气体溶解在0.2L水中(水的密度近似为1g/mL)所得溶液的密度为ρg/mL质量分数为ω,物质的量浓度为cmol/L,则下列关系中不正确的是
| A.c=1000ρω/365 | B.ω=365V/(365V+44800) |
| C.ω=365c/(1000ρ) | D.c=1000Vρ/(365V+224000) |
将30mL0.5mol/LNaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
| A.0.3mol/L | B.0.03 mol/L | C.0.05 mol/L | D.0.04 mol/L |
下列各溶液中NO3-物质的量浓度最大的是
| A.20 mL 2 moL/L Mg(NO3)2 |
| B.100 mL 2.5 mot/L NaNO3 |
| C.25 mL 1.0mol/L Al(NO3)3 |
| D.30 mL 2.5 mol/L NH4NO3 |
设NA为阿伏加德罗常数的数值,下列叙述正确的是
A.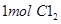 与足量Fe反应转移电子数一定为3NA 与足量Fe反应转移电子数一定为3NA |
| B.标准状况下,22.4L NH3中含有共价键的数目为NA |
C.1.0L 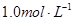 的 的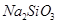 水溶液中含有的氧原子数为3NA 水溶液中含有的氧原子数为3NA |
D.4.6g Na完全转化成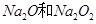 的混合物,混合物中阴离子总数为0.1NA 的混合物,混合物中阴离子总数为0.1NA |
下列有关化学用语的表示,正确的是
A.质子数为92,中子数为146的U原子: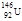 |
B.CCl4分子的比例模型: |
| C.甲醛与醋酸的最简式相同 |
D.2-甲基丁醇的结构简式: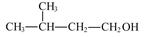 |
用NA表示阿伏加德罗常数的值。下列判断错误的是( )
| A.NA个H+的质量为1 g |
| B.2 L 0.5mol/LNa2SO4溶液中含NA个Na+ |
| C.32 g O2中含有2NA个O原子 |
| D.标准状况下,1 mol H2O中含有NA个分子 |
将一定的 、
、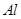 合金置于水中,结果合金完全溶解,得到20mL、PH=14的溶液,然后用1mol/L的盐酸滴定至沉淀最大时,消耗40mL盐酸。原合金中
合金置于水中,结果合金完全溶解,得到20mL、PH=14的溶液,然后用1mol/L的盐酸滴定至沉淀最大时,消耗40mL盐酸。原合金中 的物质的量( )
的物质的量( )
| A.0.01mol | B.0.02mol | C.0.03mol | D.0.04mol |
现有装有物质的量浓度为1.2 mol/L的盐酸100ml的容器甲和装有物质的量浓度为1mol/L的硫酸100ml的容器乙,向甲.乙容器内加入相同质量的铝,充分反应后生成氢气的体积比为3:4(标准状况下),问所加入的铝的质量是( )
| A.1.08克 | B.1.44克 | C.1.8 克 | D.无法计算 |