题目内容
在溶有Fe2(SO4)3和CuSO4的溶液中加入锌粉, 下列说法中不正确的是 ( )
| A.若锌粉有剩余, 则不溶物中一定有铜,可能有铁 |
| B.若锌粉有剩余, 则溶液中的金属阳离子只有Zn2+ |
| C.若锌粉无剩余, 且溶液中尚存有Cu2+, 则一定有Fe2+ |
| D.若锌粉无剩余, 且溶液中无Cu2+,则一定有Zn2+,一定无Fe3+ |
A
根据离子的氧化顺序,锌依次发生反应:①2Fe3++Zn=2Fe2++Zn2+ ②Zn+Cu2+=Zn2++Cu ③Zn+Fe2+=Zn2++Fe
A:若锌剩余,则金属铜、铁将全部被置换出,不溶物中一定有铜和铁,不正确
B:若锌剩余,所得溶液为为ZnSO4的溶液,金属阳离子只有Zn2+,正确
C:溶液中尚存有Cu2+,说明反应③还没有进行,一定有Fe2+,正确
D:溶液中无Cu2+,则反应①②已经完全进行,则溶液中一定无Fe3+,正确
A:若锌剩余,则金属铜、铁将全部被置换出,不溶物中一定有铜和铁,不正确
B:若锌剩余,所得溶液为为ZnSO4的溶液,金属阳离子只有Zn2+,正确
C:溶液中尚存有Cu2+,说明反应③还没有进行,一定有Fe2+,正确
D:溶液中无Cu2+,则反应①②已经完全进行,则溶液中一定无Fe3+,正确

练习册系列答案
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
 下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀H2SO4、
下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀H2SO4、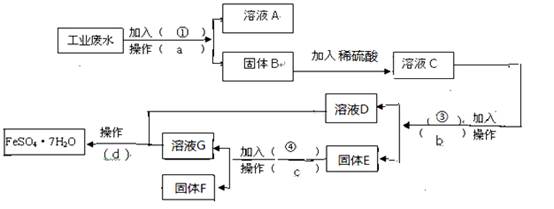 (1)操作a的名称为 ,所需要的玻璃仪器为 ____。
(1)操作a的名称为 ,所需要的玻璃仪器为 ____。 ____,加入的试剂④为 __,发生的化学方程式为 。
____,加入的试剂④为 __,发生的化学方程式为 。 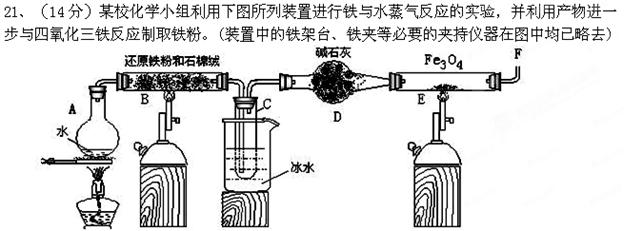
 加KSCN溶液。溶液颜色无明显变化,试解释原因 。
加KSCN溶液。溶液颜色无明显变化,试解释原因 。