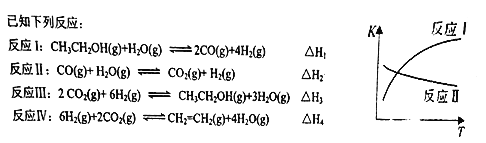
��Ŀ����
����Ŀ��Ϊ����ȼú�����к��е�SO2��NOx���о�����������������������������������ķ�����
��1����ȼú�м�������ʯ��ʯ������ʱ��SO2ת��ΪCaSO4�Ļ�ѧ����ʽ��______��
��2��ѡ���Դ���ԭ����SCR�������������ڴ����������£�ѡȡ��ԭ���������е�NO��������������NH3��ԭNO�Ļ�ѧ����ʽ��______��
��3����NaClO��Һ��Ϊ���ռ�����һ�廯��������������������������Һ��pH��5.5���������е�SO2��NOת��ΪSO42��NO3����Ϊ���ȷ�Ӧ��
������ͼ�л��������ȷ�Ӧ���ķ�Ӧ�����е������仯ʾ��ͼ��
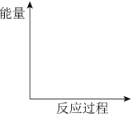
��NaClO��Һ����������SO2�����ӷ���ʽ��______��
��һ��ʱ���ڣ��¶ȶ������ѳ��ʵ�Ӱ��������ͼ��SO2���ѳ��ʸ���NO�����ܵ�ԭ����______��д��1�ּ�������
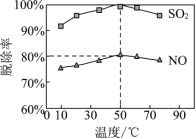
��������SO2��NO�������Ϊ4��1��50��ʱ���ѳ��ʼ�ͼ2���������Һ������ת�����ɵ�NO3��Cl�����ʵ���֮��Ϊ______��
���𰸡� 2CaCO3+2SO2+O2 ![]() 2CaSO4+2CO2 4NH3+6NO
2CaSO4+2CO2 4NH3+6NO![]() 5N2+6H2O
5N2+6H2O 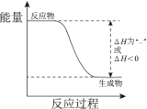
SO2+ClO+H2O == SO42+Cl+2H+
SO2��ˮ�е��ܽ�ȴ���NO SO2����Һ�еĻ�ԭ��ǿ��NO SO2��NaClO��Һ�ķ�Ӧ���ʴ���NO
2��13
����������1����ȼú�м�������ʯ��ʯ������ʱʯ��ʯ��������SO2ת��ΪCaSO4�Ļ�ѧ����ʽ��2CaCO3+2SO2+O2 ![]() 2CaSO4+2CO2����2��NH3��ԭNO���ɵ�����ˮ����Ӧ�Ļ�ѧ����ʽ��4NH3+6NO
2CaSO4+2CO2����2��NH3��ԭNO���ɵ�����ˮ����Ӧ�Ļ�ѧ����ʽ��4NH3+6NO![]() 5N2+6H2O����3���� �����ȷ�Ӧ���ķ�Ӧ�����з�Ӧ���������������������������������仯ʾ��ͼ���� ��
5N2+6H2O����3���� �����ȷ�Ӧ���ķ�Ӧ�����з�Ӧ���������������������������������仯ʾ��ͼ���� �� ����NaClO��Һ����������SO2������������ԭ��Ӧ���������ƺ����ᣬ��Ӧ�����ӷ���ʽ��SO2+ClO+H2O == SO42+Cl+2H+����һ��ʱ���ڣ��¶ȶ������ѳ��ʵ�Ӱ��������ͼ��SO2���ѳ��ʸ���NO�����ܵ�ԭ����SO2��ˮ�е��ܽ�ȴ���NO��SO2����Һ�еĻ�ԭ��ǿ��NO��SO2��NaClO��Һ�ķ�Ӧ���ʴ���NO����������SO2��NO�������Ϊ4��1��50��ʱ���ѳ��ʼ�ͼ2�ֱ�Ϊ100%��80%�����ݷ�ӦSO2+ClO+H2O == SO42+Cl+2H+��3ClO+2NO+H2O = 2NO3+3Cl+2H+���������Һ������ת�����ɵ�NO3��Cl�����ʵ���֮��Ϊ
����NaClO��Һ����������SO2������������ԭ��Ӧ���������ƺ����ᣬ��Ӧ�����ӷ���ʽ��SO2+ClO+H2O == SO42+Cl+2H+����һ��ʱ���ڣ��¶ȶ������ѳ��ʵ�Ӱ��������ͼ��SO2���ѳ��ʸ���NO�����ܵ�ԭ����SO2��ˮ�е��ܽ�ȴ���NO��SO2����Һ�еĻ�ԭ��ǿ��NO��SO2��NaClO��Һ�ķ�Ӧ���ʴ���NO����������SO2��NO�������Ϊ4��1��50��ʱ���ѳ��ʼ�ͼ2�ֱ�Ϊ100%��80%�����ݷ�ӦSO2+ClO+H2O == SO42+Cl+2H+��3ClO+2NO+H2O = 2NO3+3Cl+2H+���������Һ������ת�����ɵ�NO3��Cl�����ʵ���֮��Ϊ![]() ��
��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ��ijС���о���Һ��Fe2+��NO2��NO3�ķ�Ӧ�����ϣ� [Fe(NO)]2+����Һ�г���ɫ��
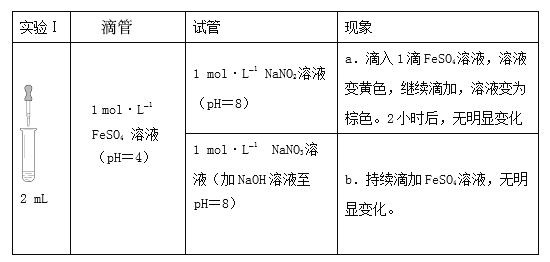
��1���о�����a�еĻ�ɫ��Һ��
����______��Һ�����Һ�к���Fe3+��
������Ϊ��O2��������Һ�е�Fe2+������ΪO2������Ҫԭ��������______��
������ʵ������װ����ͼ������ձ��е���Һֻ��Ϊ��ɫ������Ϊ��ɫ���Ҳ�缫�ϲ�����ɫ���ݣ������������ΪNO��
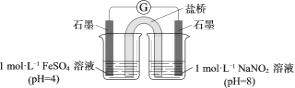
����NO�ĵ缫��Ӧʽ��______��
ʵ������Ŀ����______��
��2���о�����a�е���ɫ��Һ��
���ۺ�ʵ������ʵ������������裺����a����Һ��Ϊ��ɫ������NO����Һ�е�Fe2+��Fe3+�����˷�Ӧ������ʵ����֤ʵ��Һ����ɫֻ����ΪFe2+��NO�����˷�Ӧ��ʵ�����IJ�����������______��
������ʵ�����е���ɫ��Һ���������ݳ����������ڽӽ��Թܿڴ���Ϊ����ɫ����Һ���к��ɫ�������ɡ����Ͳ������ɫ������ԭ����______��
��3���о����������£���Һ��Fe2+��NO2��NO3�ķ�Ӧ��
��� | ���� | ���� |
�� | ȡ1 mol��L1��NaNO2��Һ���Ӵ�����pH=3������1 mol��L1FeSO4��Һ | ��Һ������Ϊ��ɫ |
�� | ȡ1 mol��L1��NaNO3��Һ���Ӵ�����pH=3������1 mol��L1FeSO4��Һ | �����Ա仯 |
�� | �ֱ�ȡ0.5 mL 1 mol��L1��NaNO3��Һ��1 mol��L1��FeSO4��Һ����ϣ�С�ļ���0.5 mLŨ���� | Һ���Ϊ���㣬�Ժ�������Һ������ϳ�����ɫ�� |
�٢�����Һ��Ϊ��ɫ�����ӷ���ʽ��______��______��
�ڢ��г�����ɫ��ԭ����______��
ʵ����ۣ���ʵ������������Һ��NO2��NO3������������Һ������Ե��йء�