题目内容
在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100 mol/L、c(B)=0.200 mol/L及c(C)=0 mol/L。反应物A的浓度随时间的变化如下图所示。
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100 mol/L、c(B)=0.200 mol/L及c(C)=0 mol/L。反应物A的浓度随时间的变化如下图所示。
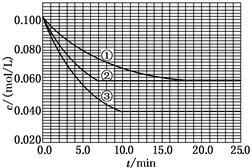
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②______________________________________________;
③______________________________________________;
(2)实验②平衡时B的转化率为________;实验③平衡时C的浓度为________________;
(3)该反应的ΔH________0,其判断理由是_________________________________;
(4)该反应进行到4.0 min时的平均反应速率:
实验②:vB=________;
实验③:vC=________。
 C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100 mol/L、c(B)=0.200 mol/L及c(C)=0 mol/L。反应物A的浓度随时间的变化如下图所示。
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100 mol/L、c(B)=0.200 mol/L及c(C)=0 mol/L。反应物A的浓度随时间的变化如下图所示。
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②______________________________________________;
③______________________________________________;
(2)实验②平衡时B的转化率为________;实验③平衡时C的浓度为________________;
(3)该反应的ΔH________0,其判断理由是_________________________________;
(4)该反应进行到4.0 min时的平均反应速率:
实验②:vB=________;
实验③:vC=________。
(1)②加催化剂 达到平衡的时间缩短,平衡时A的浓度未变 ③温度升高 达到平衡的时间缩短,平衡时A的浓度减小
(2)40%(或0.4) 0.060 mol/L
(3)> 温度升高,平衡向正反应方向移动,故该反应是吸热反应
(4)0.014 mol/(L·min) 0.009 mol/(L·min)
(2)40%(或0.4) 0.060 mol/L
(3)> 温度升高,平衡向正反应方向移动,故该反应是吸热反应
(4)0.014 mol/(L·min) 0.009 mol/(L·min)
本题主要考查化学平衡,意在考查考生读图、表述和计算能力。(1)分析图像可知,①和②在平衡时刻A的浓度相等,且②的曲线斜率较大,说明反应速率较大,故是改变某一条件使反应加快,但平衡没有移动,故只可能是使用了催化剂。①和③相比较,平衡时刻③中A的浓度较小,曲线斜率较大,说明③的反应速率较大且平衡向正方向移动,而起始浓度相等,故只可能是升高温度。
(2)由起始到平衡时刻Δc(A)=0.10 mol·L-1-0.060 mol·L-1=0.040 mol·L-1,故Δc(B)=0.080 mol·L-1,则B的转化率为0.080÷0.20×100%=40%;实验③平衡时刻,c(C)=0.060 mol·L-1。
(3)由(1)可知,温度升高平衡向正方向移动,那么该反应正反应方向要吸热,ΔH>0。
(4)观察图像可知,在第4.0 min时,②中c(A)=0.072 mol·L-1,③中c(A)=0.064 mol·L-1。②中v(A)=(0.10 mol·L-1-0.072 mol·L-1)/4.0 min=0.007 mol·L-1·min-1,而v(B)=2v(A)=0.014 mol·L-1·min-1。③中v(A)=(0.1 mol·L-1-0.064 mol·L-1)/4.0 min=0.009 mol·L-1·min-1,而v(C)=v(A)=0.009 mol·L-1·min-1。
(2)由起始到平衡时刻Δc(A)=0.10 mol·L-1-0.060 mol·L-1=0.040 mol·L-1,故Δc(B)=0.080 mol·L-1,则B的转化率为0.080÷0.20×100%=40%;实验③平衡时刻,c(C)=0.060 mol·L-1。
(3)由(1)可知,温度升高平衡向正方向移动,那么该反应正反应方向要吸热,ΔH>0。
(4)观察图像可知,在第4.0 min时,②中c(A)=0.072 mol·L-1,③中c(A)=0.064 mol·L-1。②中v(A)=(0.10 mol·L-1-0.072 mol·L-1)/4.0 min=0.007 mol·L-1·min-1,而v(B)=2v(A)=0.014 mol·L-1·min-1。③中v(A)=(0.1 mol·L-1-0.064 mol·L-1)/4.0 min=0.009 mol·L-1·min-1,而v(C)=v(A)=0.009 mol·L-1·min-1。

练习册系列答案
相关题目
 CO(g)+3H2(g)……Ⅰ,CH4的转化率与温度、压强的关系如图所示。
CO(g)+3H2(g)……Ⅰ,CH4的转化率与温度、压强的关系如图所示。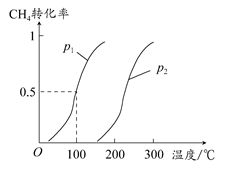
 CH3OH (g) DH1
CH3OH (g) DH1 C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol/L、c(B )="0.200" mol/L及c(C )="0" mol/L。反应物A的浓度随时间的变化如图所示。
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol/L、c(B )="0.200" mol/L及c(C )="0" mol/L。反应物A的浓度随时间的变化如图所示。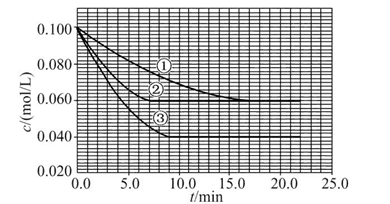
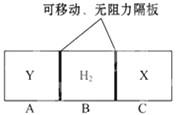
 Y(g) + Z(g) △H<0,反应一段时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示。下列说法中不正确的是
Y(g) + Z(g) △H<0,反应一段时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示。下列说法中不正确的是