题目内容
向明矾溶液中滴入氢氧化钡溶液,当硫酸根离子恰好完全沉淀时,铝元素的存在形式是
[ ]
A.一部分为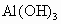 ,一部分为
,一部分为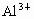
B.一部分为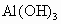 ,一部分为
,一部分为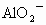
C.全部是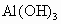
D.全部是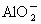
答案:D

练习册系列答案
相关题目
下表中对离子方程式的评价不合理的是
| 选项 | 化学反应及其离子方程式 | 评价 |
| A. | 向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全2Al3++3SO42- +3Ba2++6OH-=3BaSO4↓+2 Al(OH)3↓ | 不正确 |
| B. | 向碳酸氢钠溶液中滴入过量石灰水:2HCO3-+Ca2++2OH-= CaCO3↓+2H2O+ CO32- | 正确 |
| C. | 铁粉与稀硫酸反应: 2Fe+ 6H+ ="=" 2Fe3+ + 3H2↑ | 不正确, H+的氧化性较弱,只能将铁单质氧化为Fe2+ |
| D. | 向硫酸铵溶液中加入氢氧化钡溶液: Ba2+ + SO42- ="=" BaSO4↓ | 不正确 |
下表中对离子方程式的评价不合理的是
|
选项 |
化学反应及其离子方程式 |
评价 |
|
A. |
向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全2Al3++3SO42- +3Ba2++6OH-=3BaSO4↓+2 Al(OH)3↓ |
不正确 |
|
B. |
向碳酸氢钠溶液中滴入过量石灰水:2HCO3-+Ca2++2OH-= CaCO3↓+2H2O+ CO32- |
正确 |
|
C. |
铁粉与稀硫酸反应: 2Fe+ 6H+ == 2Fe3+ + 3H2↑ |
不正确, H+的氧化性较弱,只能将铁单质氧化为Fe2+ |
|
D. |
向硫酸铵溶液中加入氢氧化钡溶液: Ba2+ + SO42- == BaSO4↓ |
不正确 |
下表中对离子方程式的评价不合理的是
| 选项 | 化学反应及其离子方程式 | 评价 |
| A. | 向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全2Al3++3SO42- +3Ba2++6OH-=3BaSO4↓+2 Al(OH)3↓ | 不正确 |
| B. | 向碳酸氢钠溶液中滴入过量石灰水:2HCO3-+Ca2++2OH-= CaCO3↓+2H2O+ CO32- | 正确 |
| C. | 铁粉与稀硫酸反应: 2Fe+ 6H+ == 2Fe3+ + 3H2↑ | 不正确, H+的氧化性较弱,只能将铁单质氧化为Fe2+ |
| D. | 向硫酸铵溶液中加入氢氧化钡溶液: Ba2+ + SO42- == BaSO4↓ | 不正确 |