题目内容
在一定条件下可实现下列物质间的转化,如下图所示:
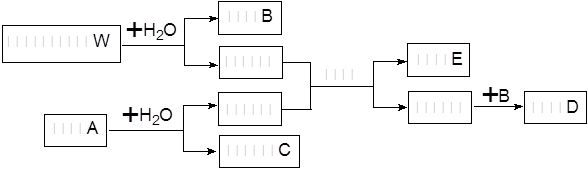
(1)固体A是一种重要的工业原料,其化学式为____________________。W的电子式为_____ ____
(2)写出W与气体丙反应的化学方程式___________________________
(3)利用上图中有关物质实现C→B的转变,写出该转变的离子方程式:__________ _____
(4)上述变化中的B和丙按物质的量3:2反应的离子方程式为:_______。
(5)若甲和乙恰好完全反应,则W与A的物质的量之比为_______。
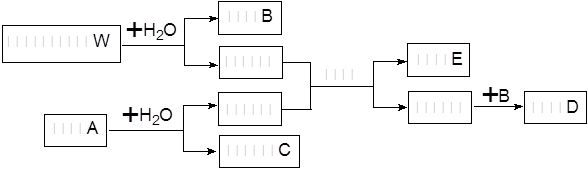
(1)固体A是一种重要的工业原料,其化学式为____________________。W的电子式为_____ ____
(2)写出W与气体丙反应的化学方程式___________________________
(3)利用上图中有关物质实现C→B的转变,写出该转变的离子方程式:__________ _____
(4)上述变化中的B和丙按物质的量3:2反应的离子方程式为:_______。
(5)若甲和乙恰好完全反应,则W与A的物质的量之比为_______。
(1)CaC2 , 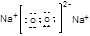
(2)2Na2O2+2CO2=2Na2CO3+O2
(3)Ca(OH)2+CO32-=CaCO3+2OH-
(4)3OH-+2CO2=HCO3-+CO32-+H2O
(5)5:1
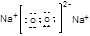
(2)2Na2O2+2CO2=2Na2CO3+O2
(3)Ca(OH)2+CO32-=CaCO3+2OH-
(4)3OH-+2CO2=HCO3-+CO32-+H2O
(5)5:1
试题分析:浅黄色固体和水反应放出气体,可以推断出W是Na2O2,B是NaOH,甲是氧气,气体丙也能和Na2O2反应,说明丙是CO2,E是水,则气体乙应该是烃或烃的含氧衍生物,能和水反应生成乙可以推断出实验室制备乙炔,A是CaC2,C是氢氧化钙。(4)根据电荷守恒和原子个数守恒可以写出3OH-+2CO2=HCO3-+CO32-+H2O,(5)2Na2O2产生1摩尔氧气,1摩尔乙炔燃烧需要2.5molO2,需要CaC2原料1摩尔,由此可以计算出结果5:1

练习册系列答案
相关题目
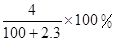
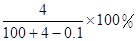
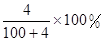
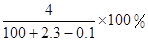
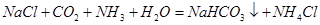 ”是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是
”是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是