题目内容
【题目】A、J是日常生活中常见的两种金属,J在化合物中存在两种正价;F是常温下的气体单质,各物质有以下的转化关系(部分产物及条件略去). 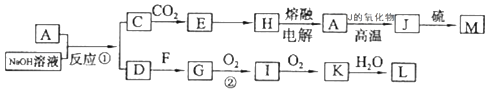
(1)A与NaOH溶液反应的离子方程式为;方程式中氧化剂为 .
(2)写出L的稀溶液与足量的J反应的化学方程式 .
(3)含A元素的某盐X常做净水剂,X做焰色反应时,透过蓝色钴玻璃观察火焰呈紫色.X的水溶液与NaHCO3溶液混合,反应的离子方程式为 .
【答案】
(1)2Al+2H2O+2OH﹣=2AlO2﹣+3H2↑;H2O
(2)3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O
(3)Al3++3HCO3﹣=Al(OH)3+3CO2↑
【解析】解:(1)Al与氢氧化钠溶液反应离子方程式为:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑,反应中水为氧化剂, 所以答案是:2Al+2H2O+2OH﹣=2AlO2﹣+3H2↑;H2O;(2)稀硝酸溶液与足量铁反应生成硝酸亚铁和NO,化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,
所以答案是:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O;(3)含Al元素的某盐X常做净水剂,X做焰色反应时,透过蓝色钴玻璃观察火焰呈紫色,说明含有钾元素,判断X为KAl(SO4)2 , X的水溶液与NaHCO3溶液混合,铝离子和碳酸氢根离子水溶液中双水解反应生成氢氧化铝沉淀和二氧化碳,反应的离子方程式为:Al3++3HCO3﹣=Al(OH)3↓+3CO2↑,
所以答案是:Al3++3HCO3﹣=Al(OH)3+3CO2↑.

练习册系列答案
相关题目