题目内容
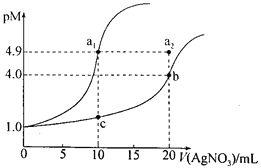
【题目】某温度下,向10 mL 0.1 mol·L-lNaCl溶液和10 mL 0.1 mol·L-lK2CrO4溶液中分别滴加0.1 mol·L-lAgNO3溶液。滴加过程中pM[-lgc(Cl-)或-lgc(CrO42-)]与所加AgNO3溶液体积之间的关系如下图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
A. 该温度下,Ksp(Ag2CrO4)=4×10-12
B. al、b、c三点所示溶液中c(Ag+):al>b>c
C. 若将上述NaCl溶液浓度改为0.2mol·L-1,则a1点会平移至a2点
D. 用AgNO3标准溶液滴定NaCl溶液时,可用K2CrO4溶液作指示剂
【答案】B
【解析】
根据pM=-lgc(Cl-)或pM=-lgc(CrO42-)可知,c(CrO42-)越小,pM越大,根据图像,向10 mL 0.1 mol·L-lNaCl溶液和10 mL 0.1 mol·L-lK2CrO4溶液中分别滴加0.1 mol·L-lAgNO3溶液。当滴加10 mL0.1 mol·L-lAgNO3溶液时,氯化钠恰好反应,滴加20 mL0.1 mol·L-lAgNO3溶液时,K2CrO4恰好反应,因此al所在曲线为氯化钠,b、c所在曲线为K2CrO4,据此分析解答。
A.b点时恰好反应生成Ag2CrO4,-lgc(CrO42-)=4.0,c(CrO42-)= 10-4mol·L-l,则c(Ag+)=2× 10-4mol·L-l,该温度下,Ksp(Ag2CrO4)=c(CrO42-)×c2(Ag+)=4×10-12,故A正确;
B.al点恰好反应,-lgc(Cl-)=4.9,c(Cl-)=10-4.9mol·L-l,则c(Ag+)=10-4.9mol·L-l,b点c(Ag+)=2× 10-4mol·L-l,c点,K2CrO4过量,c(CrO42-)约为原来的![]() ,则c(CrO42-)= 0.025mol·L-l,则c(Ag+)=
,则c(CrO42-)= 0.025mol·L-l,则c(Ag+)=![]() =
=![]() ×10-5mol·L-l,al、b、c三点所示溶液中b点的c(Ag+)最大,故B错误;
×10-5mol·L-l,al、b、c三点所示溶液中b点的c(Ag+)最大,故B错误;
C.温度不变,氯化银的溶度积不变,若将上述NaCl溶液浓度改为0.2mol·L-1,平衡时,-lgc(Cl-)=4.9,但需要的硝酸银溶液的体积变成原来的2倍,因此a1点会平移至a2点,故C正确;
D.根据上述分析,当溶液中同时存在Cl-和CrO42-时,加入硝酸银溶液,Cl-先沉淀,用AgNO3标准溶液滴定NaCl溶液时,可用K2CrO4溶液作指示剂,滴定至终点时,会生成Ag2CrO4为红棕色沉淀,故D正确;
答案选B。

 天天向上口算本系列答案
天天向上口算本系列答案