题目内容
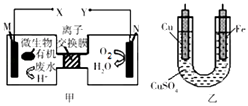
【题目】亚硝酸钠是重要的防腐剂.某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠.(夹持装置和A中加热装置已略,气密性已检验),查阅资料:
①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②在酸性溶液中,NO2﹣可将MnO4﹣还原为Mn2+ .
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
实验操作:①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热;③从C中取少量固体,检验是否是亚硝酸钠.
回答下列问题:
(1)装置中仪器a的名称为;D装置的作用是 .
(2)A中反应的化学方程式是;C中反应生成NaNO2的化学方程式是 .
(3)检验C中产物有亚硝酸钠的正确操作是 .
a.取少量生成物溶于水充分振荡,滴加酚酞试液,若溶液变红,则含有NaNO2 .
b.取少量生成物溶于稀硫酸,若产生无色气体并在液体上方变为红棕色,则含有NaNO2 .
(4)经检验C产物中亚硝酸钠含量较少.
①.甲同学认为C中产物不仅有亚硝酸钠,还可能有其它固体物质.为排除干扰,甲在B、C装置间增加装置E,E中盛放的试剂应是(写名称).
②.乙同学认为除上述干扰因素外,还会有空气参与反应导致产品不纯,所以在实验操作①前应增加一步操作,该操作是 .
【答案】
(1)分液漏斗;除去未反应的NO,防止污染空气
(2)C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O;2NO+Na2O2=2NaNO2
CO2↑+4NO2↑+2H2O;2NO+Na2O2=2NaNO2
(3)b
(4)碱石灰;打开弹簧夹,通入N2一段时间
【解析】解:(1)a名称是分液漏斗;NO有毒不能直接排空,NO和酸性高锰酸钾溶液反应生成硝酸根离子和锰离子,从而除去NO,所以答案是:分液漏斗;除去未反应的NO,防止污染空气;(2)C和HNO3(浓)发生反应生成CO2、NO2、H2O,反应方程式为C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O;NO和Na2O2发生反应生成NaNO2 , 反应方程式为 2NO+Na2O2=2NaNO2 ,
CO2↑+4NO2↑+2H2O;NO和Na2O2发生反应生成NaNO2 , 反应方程式为 2NO+Na2O2=2NaNO2 ,
所以答案是:C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O;2NO+Na2O2=2NaNO2;(3)a.A中生成二氧化碳,二氧化碳和过氧化钠反应生成碳酸钠,碳酸钠溶液也呈碱性,B中出来的气体中还含有水蒸气能和C中的过氧化钠反应生成NaOH而呈碱性,所以不能根据其水溶液判断含有亚硝酸钠,故a错误;
CO2↑+4NO2↑+2H2O;2NO+Na2O2=2NaNO2;(3)a.A中生成二氧化碳,二氧化碳和过氧化钠反应生成碳酸钠,碳酸钠溶液也呈碱性,B中出来的气体中还含有水蒸气能和C中的过氧化钠反应生成NaOH而呈碱性,所以不能根据其水溶液判断含有亚硝酸钠,故a错误;
b.亚硝酸钠能和稀硫酸反应生成无色气体NO,NO不稳定易被氧气氧化生成红棕色气体二氧化氮,该实验现象说明含有亚硝酸钠,故b正确;
故选:b;(4)①从B装置中出来的气体中含有NO、二氧化碳和水蒸气,这几种物质都能和过氧化钠反应,要使C中只有NO和过氧化钠反应,则BC装置间的E装置应该能吸收水蒸气和二氧化碳,使用的药品是碱石灰,
所以答案是:碱石灰;
②要排除空气防止发生反应,应该先通入一段时间的氮气,所以答案是:打开弹簧夹,通入N2一段时间.