题目内容
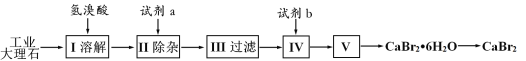
【题目】溴化钙可用作阻燃剂、制冷剂,具有易溶于水,易吸潮等性质。实验室用工业大理石(含有少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下:
下列说法错误的是
A.已知步骤Ⅲ的滤液中不含NH4+,步骤II加入的试剂a是石灰水
B.步骤II控制溶液的pH约为8.0的主要目的是沉淀过量Ca2+
C.试剂b是氢溴酸,步骤IV的目的是除去过量的氢氧化钙
D.步骤V所含的操作依次是蒸发浓缩,冷却结晶
【答案】B
【解析】
大理石和氢溴酸反应生成溴化钙,因含有少量Al3+、Fe3+等杂质,可加入石灰水,沉淀Al3+、Fe3+,过滤后得到溴化钙、氢氧化钙的混合溶液,加入试剂b为氢溴酸,可除去过量的氢氧化钙,然后经蒸发浓缩、冷却结晶可得到溴化钙晶体,据此分析解答。
A.已知步骤Ⅲ的滤液中不含NH4+,步骤II加入的试剂a的目的是防止氢氧化铝溶解,因此a是碱,根据题意及不引入新的杂质可知是氢氧化钙,故A正确;
B.步骤II控制溶液的pH约为8.0的主要目的是沉淀Al3+、Fe3+,故B错误;
C.加试剂b的目的是除去过量的氢氧化钙,且不引入新杂质,可以加入氢溴酸,故C正确;
D.步骤Ⅴ的结果是从溶液中得到CaBr26H2O,因此其操作步骤为蒸发浓缩,冷却结晶、过滤,故D正确;
答案选B。

练习册系列答案
相关题目
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 稀硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | KMnO4 | Cl2 | NaOH溶液 |
A.AB.BC.CD.D