题目内容
有A、B、C、D、E、F六瓶未知溶液.它们是MgSO4、BaCl2、(NH4)2CO3、AgNO3、HBr和NaOH.为了鉴别,各取少许溶液进行两两混和试验,结果如右表.表中“↓“表示有沉淀或生成微溶化合物,“↑“表示有气体生成,“-“表示观察不到明显的现象变化.由此可以判断:
A是________、B是________、C是________、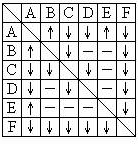
D是________、E是________、F是________.
(NH4)2CO3 NaOH MgSO4 BaCl2 HBr AgNO3
分析:根据反应现象最多或最少的物质推断.F与其他四种物质均生成沉淀,可推出F;只有碳酸铵与氢溴酸反应生成气体,A与气体四种物质反应均有现象,与E还有气体生成,可推出A、E,再据现象推出气体物质.
解答:F与其他四种物质均生成沉淀,所以F为硝酸银;A与D均生成生成三种沉淀,A还与E生成气体,所以A为碳酸铵、E为氢溴酸、D为氯化钡;B生成两种沉淀且与A生成气体,则B为氢氧化钠,C为硫酸镁.
故答案为:(NH4)2CO3;NaOH;MgSO4;BaCl2;HBr;AgNO3.
点评:本题主要是利用现象推断物质,主要考查物质的性质,解题时要充分分析反应现象.
分析:根据反应现象最多或最少的物质推断.F与其他四种物质均生成沉淀,可推出F;只有碳酸铵与氢溴酸反应生成气体,A与气体四种物质反应均有现象,与E还有气体生成,可推出A、E,再据现象推出气体物质.
解答:F与其他四种物质均生成沉淀,所以F为硝酸银;A与D均生成生成三种沉淀,A还与E生成气体,所以A为碳酸铵、E为氢溴酸、D为氯化钡;B生成两种沉淀且与A生成气体,则B为氢氧化钠,C为硫酸镁.
故答案为:(NH4)2CO3;NaOH;MgSO4;BaCl2;HBr;AgNO3.
点评:本题主要是利用现象推断物质,主要考查物质的性质,解题时要充分分析反应现象.

练习册系列答案
相关题目