题目内容
【题目】![]() 的
的![]() 溶液加水稀释100倍后,pH______
溶液加水稀释100倍后,pH______![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() ,原因是______
,原因是______![]() 用离子方程式和必要的文字说明
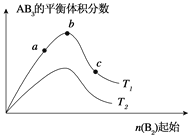
用离子方程式和必要的文字说明![]() ;pH相等的NaOH溶液与
;pH相等的NaOH溶液与![]() 溶液,分别加热到相同的温度后
溶液,分别加热到相同的温度后![]() 溶液的pH______NaOH溶液的
溶液的pH______NaOH溶液的![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() ;
;
![]() 相等时,
相等时,![]() 三种溶液中
三种溶液中![]() 由大到小的顺序为______;
由大到小的顺序为______;
![]() 等体积、等浓度的氢氧化钠与醋酸混合后溶液呈 ______ 性,溶液中
等体积、等浓度的氢氧化钠与醋酸混合后溶液呈 ______ 性,溶液中![]() ______
______ ![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() ;
;![]() 的氢氧化钠与
的氢氧化钠与![]() 的醋酸等体积混合后溶液呈______性,溶液中
的醋酸等体积混合后溶液呈______性,溶液中![]() ______
______ ![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() ;
;
![]() ,用
,用![]() 溶液滴定
溶液滴定![]() 某一元酸HA溶液所得滴定曲线如图。
某一元酸HA溶液所得滴定曲线如图。
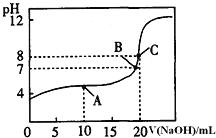
![]() 为减小实验误差,由图可知滴定时指示剂应选用______
为减小实验误差,由图可知滴定时指示剂应选用______![]() 填“石蕊”、“酚酞”、“甲基橙”
填“石蕊”、“酚酞”、“甲基橙”![]() ;
;
![]() 、B、C三点所示溶液导电能力最强的是 ______ 点对应的溶液;
、B、C三点所示溶液导电能力最强的是 ______ 点对应的溶液;
![]() ,A点的离子浓度大小关系是 ______ .
,A点的离子浓度大小关系是 ______ .
【答案】![]() CH3COO-+H2O
CH3COO-+H2O![]() CH3COOH+OH-,加水稀释后醋酸根离子的水解程度增大,产生
CH3COOH+OH-,加水稀释后醋酸根离子的水解程度增大,产生![]() 增多,抵消掉部分溶液体积增大的影响,则溶液的
增多,抵消掉部分溶液体积增大的影响,则溶液的![]()
![]()
![]() 碱
碱 ![]() 酸
酸 ![]() 酚酞 C
酚酞 C ![]()
【解析】
(1)醋酸根离子水解溶液显碱性,![]() ,加水稀释后醋酸根离子的水解程度增大;pH相等的NaOH溶液与
,加水稀释后醋酸根离子的水解程度增大;pH相等的NaOH溶液与![]() 溶液,醋酸钠为强碱弱酸盐,加热后醋酸根离子的水解程度增大,以此解答;
溶液,醋酸钠为强碱弱酸盐,加热后醋酸根离子的水解程度增大,以此解答;
(2)相同pH的![]() 与
与![]() 溶液,
溶液,![]() 与
与![]() 都是强酸弱碱盐,根据溶液呈电中性可判断二者
都是强酸弱碱盐,根据溶液呈电中性可判断二者![]() 浓度相等,由于
浓度相等,由于![]() 电离时产生
电离时产生![]() 使溶液呈酸性,
使溶液呈酸性,![]() 的水解被抑制,以此判断;
的水解被抑制,以此判断;
(3)等体积、等浓度的氢氧化钠与醋酸混合,恰好反应生成醋酸钠溶液,溶液中的醋酸根离子水解溶液显碱性,钠离子浓度大于醋酸根离子,![]() ,
,![]() 的氢氧化钠与
的氢氧化钠与![]() 的醋酸溶液中氢氧根离子浓度和氢离子浓度相同;
的醋酸溶液中氢氧根离子浓度和氢离子浓度相同;
(4)碱性变色范围内的指示剂是酚酞,C点恰好反应生成盐,离子浓度最大,导电能力最强,以此判断。
![]() 的
的![]() 溶液加水稀释100倍后,由于醋酸根离子水解溶液显碱性,
溶液加水稀释100倍后,由于醋酸根离子水解溶液显碱性,![]() ,加水稀释后醋酸根离子的水解程度增大,产生
,加水稀释后醋酸根离子的水解程度增大,产生![]() 增多,抵消掉部分溶液体积增大的影响,则溶液的
增多,抵消掉部分溶液体积增大的影响,则溶液的![]() ;pH相等的NaOH溶液与
;pH相等的NaOH溶液与![]() 溶液,醋酸钠为强碱弱酸盐,加热后醋酸根离子的水解程度增大,则溶液pH增大,所以分别加热到相同的温度后
溶液,醋酸钠为强碱弱酸盐,加热后醋酸根离子的水解程度增大,则溶液pH增大,所以分别加热到相同的温度后![]() 溶液的
溶液的![]() 溶液的pH,故答案为:
溶液的pH,故答案为:![]() ;
;![]() ,加水稀释后醋酸根离子的水解程度增大,产生
,加水稀释后醋酸根离子的水解程度增大,产生![]() 增多,抵消掉部分溶液体积增大的影响,则溶液的
增多,抵消掉部分溶液体积增大的影响,则溶液的![]() ;
;![]() ;
;
![]() 相同pH的
相同pH的![]() 与
与![]() 溶液,
溶液,![]() 与
与![]() 都是强酸弱碱盐,根据溶液呈电中性可判断二者
都是强酸弱碱盐,根据溶液呈电中性可判断二者![]() 浓度相等,由于
浓度相等,由于![]() 电离时产生
电离时产生![]() 使溶液呈酸性,
使溶液呈酸性,![]() 的水解被抑制,因此
的水解被抑制,因此![]() 中
中![]() 的浓度小于
的浓度小于![]() ,则溶液中铵根离子浓度大小为:
,则溶液中铵根离子浓度大小为:![]() ,故答案为:
,故答案为:![]() ;
;
![]() 等体积、等浓度的氢氧化钠与醋酸混合,恰好反应生成醋酸钠溶液,溶液中的醋酸根离子水解溶液显碱性,钠离子浓度大于醋酸根离子,
等体积、等浓度的氢氧化钠与醋酸混合,恰好反应生成醋酸钠溶液,溶液中的醋酸根离子水解溶液显碱性,钠离子浓度大于醋酸根离子,![]() ,
,![]() 的氢氧化钠与
的氢氧化钠与![]() 的醋酸溶液中氢氧根离子浓度和氢离子浓度相同,等体积混合后醋酸又电离出氢离子,溶液显酸性,醋酸根离子浓度大于钠离子浓度,
的醋酸溶液中氢氧根离子浓度和氢离子浓度相同,等体积混合后醋酸又电离出氢离子,溶液显酸性,醋酸根离子浓度大于钠离子浓度,![]() ,故答案为:碱;
,故答案为:碱;![]() ;酸;
;酸;![]() ;
;
![]() 由图两者恰好完全反应,溶液呈碱性,应选择碱性变色范围内的指示剂是酚酞,C点恰好反应生成盐,离子浓度最大,导电能力最强;A点时,溶液中的溶质为等浓度的NaA和HA,溶液呈酸性,所以HA的电离程度大于
由图两者恰好完全反应,溶液呈碱性,应选择碱性变色范围内的指示剂是酚酞,C点恰好反应生成盐,离子浓度最大,导电能力最强;A点时,溶液中的溶质为等浓度的NaA和HA,溶液呈酸性,所以HA的电离程度大于![]() 的水解程度,所以溶液中离子浓度大小的关系为
的水解程度,所以溶液中离子浓度大小的关系为![]() ,故答案为:
,故答案为:![]() 酚酞;
酚酞;![]() ;
;![]()

【题目】氢叠氮酸(HN3)和莫尔盐(NH4)2SO4·FeSO4·6H2O是两种常用原料。
(1)氨叠氮酸易溶于水,25℃时,该酸的电离常数为Ka=10×10-5
①氢叠氮酸在水溶液中的电离方程式为________________________________
②0.2mol/L的HN3溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃,混合溶液中各离子和HN3分子浓度由大到小的顺序为__________________________。
③已知T℃时,Ksp(CuN3)=5.0×10-9,Ksp(Cu2S)=2.5×10-48,则相同温度下,2CuN3(s)+S2-(aq)![]() Cu2S(s)+2N3-(aq)该反应正反应方向_________(“能”或“不能”)进行基本彻底,请通过计算说明_________________________。
Cu2S(s)+2N3-(aq)该反应正反应方向_________(“能”或“不能”)进行基本彻底,请通过计算说明_________________________。
(2)在FeSO4溶液中,加入(NH4)2SO4固体可制备莫尔盐晶体,为了测定产品纯度,称取ag产品溶于水,配制成500mL溶液,用浓度为cmol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如下:(已知莫尔盐的分子量为392)
实验次数 | 第一次 | 第二次 | 第三次 |
消耗KMnO4溶液体积/mL | 25.52 | 25.02 | 24.98 |
滴定终点的现象是________________,通过实验数据,计算该产品的纯度为_________(用含字母a、c的式子表示)。上表第一次实验中记录数据明显大于后两次,其原因可能是_________。
A.第一次滴定时,锥形瓶用待装液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失