题目内容
运用已有知识,比较Na与Fe的性质。
| 物质 | 钠 | 铁 | |
| 物理 | 相同点 | 都是______________色金属,常温下都是____________体 | |
| 性质 | 不同点 | 密度、硬度、熔沸点比较________ | 密度、硬度、熔沸点比较____ |
| 化学性质 点 | 相同点 | 都能与O2等非金属反应,都能置换出酸中的氢。在点燃条件下Na、Fe与氧气反应的方程式分别为__________、__________;与盐酸反应的方程式分别为__________________、______________ | |
| 不同点 | Na与水反应剧烈,方程式为________ | Fe与水常温下不反应,与水蒸气反应,方程式为______ |
.银白 固 低 高 2Na+O2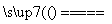 Na2O2 3Fe+2O2
Na2O2 3Fe+2O2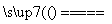 Fe3O4 2Na+2HCl===2NaCl+H2↑ Fe+2HCl===FeCl2+H2↑ 2Na+2H2O===2NaOH+H2↑ 3Fe+4H2O(g)
Fe3O4 2Na+2HCl===2NaCl+H2↑ Fe+2HCl===FeCl2+H2↑ 2Na+2H2O===2NaOH+H2↑ 3Fe+4H2O(g)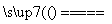 Fe3O4+4H2
Fe3O4+4H2

 阅读快车系列答案
阅读快车系列答案某课外小组设计了下图所示的实验装置(图中固定装置已略去),进行SO2性质的研究。
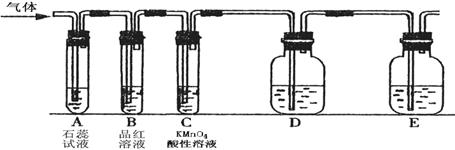 |
(1)从物质分类的角度,SO2属于 (填“酸性”或“碱性”)氧化物。写出硫酸型酸雨形成的反应方程式: 。
① 图中D装置可用来验证SO2具有该性质,其中所加入的试剂是 。
② 当向该装置通入SO2时,A中紫色石蕊溶液变红,用化学用语解释其原因是 。(2)从元素化合价的角度分析,SO2的性质。
①当向该装置通入SO2 一段时间后,可观察C中溶液褪色,MnO4-转化为Mn2+,说明SO2具有 性,反应的离子方程式为 。
②如验证SO2还具有另一方面的性质,可选择的药品是 。
A.过氧化氢 B. 浓硫酸 C.氯水 D.硫化钠溶液
 浓度为( )
浓度为( )