题目内容
用电弧法合成的储氢纳米碳管常伴有大量的碳纳米顺粒(杂质),这种颗粒可用氧化气化法提纯,其反应式为:(1)完成配平上述反应的化学方程式:
(2)反应的氧化剂是
(3)H2SO4在上述反应中表现出来的性质是
A酸性 B氧化性 C吸水性 D脱水性
(4)上述反应中若产生0.2molCO2气体,则转移电子的物质的量是
分析:(1)反应中C元素的化合价由0升高为+4价,Cr元素的化合价由+6价降低为+3价,结合质量守恒定律以此配平,并计算转移的电子数;
(2)氧化产物是化合价升高元素所在的产物,根据二氧化碳的结构来回答;
(3)该反应中,硫酸中各元素的化合价不发生变化,据此来判断性质;
(4)根据电子转移情况结合二氧化碳量来进行回答.
(2)氧化产物是化合价升高元素所在的产物,根据二氧化碳的结构来回答;
(3)该反应中,硫酸中各元素的化合价不发生变化,据此来判断性质;
(4)根据电子转移情况结合二氧化碳量来进行回答.
解答:解:(1)反应中C元素的化合价由0升高为+4价,Cr元素的化合价由+6价降低为+3价,由电子守恒可知,C的化学计量数为3,K2Cr2O7的化学计量数为2,由质量守恒定律可知,配平后的化学反应为3C+2K2Cr2O7+8H2SO4=3CO2+2K2SO4+2Cr2(SO4)3+8H2O,故答案为:3;2;8;3;2;2;8;
(2)Cr元素的化合价降低,则K2Cr2O7为氧化剂,氧化产物是二氧化碳,二氧化碳中,碳原子和氧原子之间通过共价双键结合,属于非极性分子,它的电子式为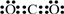 ,故答案为:K2Cr2O7;
,故答案为:K2Cr2O7;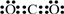 ;
;
(3)该反应中,硫酸中各元素的化合价不发生变化,反应中生成硫酸盐,则硫酸在该反应中作酸,体现酸性,应选A,故选A;
(4)化学反应中,1molC参加反应生成1mol二氧化碳时转移电子为1mol×(4-0)=4mol,所以若产生0.2molCO2气体,则转移电子的物质的量是0.8mol,故答案为:0.8.
(2)Cr元素的化合价降低,则K2Cr2O7为氧化剂,氧化产物是二氧化碳,二氧化碳中,碳原子和氧原子之间通过共价双键结合,属于非极性分子,它的电子式为
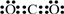 ,故答案为:K2Cr2O7;
,故答案为:K2Cr2O7;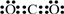 ;
; (3)该反应中,硫酸中各元素的化合价不发生变化,反应中生成硫酸盐,则硫酸在该反应中作酸,体现酸性,应选A,故选A;
(4)化学反应中,1molC参加反应生成1mol二氧化碳时转移电子为1mol×(4-0)=4mol,所以若产生0.2molCO2气体,则转移电子的物质的量是0.8mol,故答案为:0.8.
点评:本题考查氧化还原反应,明确常见元素的化合价及反应中元素的化合价变化是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
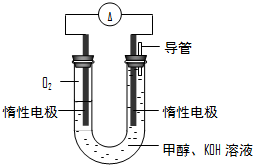 (2013?上饶一模)“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题
(2013?上饶一模)“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题