题目内容
| |||||||||||
解析:
(1) |
淡黄色固体变为白色;CO2+Ca2++2OH-=CaCO3↓+H2O;C装置中收集到O2 |
(2) |
烧瓶内壁产生水雾和黄色固体,烧瓶中形成喷泉(或NaOH溶液进入烧瓶),且溶液几乎充满烧瓶,SO2+2 H2S=3 S=2 H2O,烧瓶内产生大量白烟,烧瓶中形成喷泉(或NaOH溶液进入烧瓶),且溶液充满烧瓶,NH3+HCl=NH4Cl,烧瓶内气体由无色变为红棕色,有溶液进入烧瓶,但未充满,气体由红棕色变为无色,2 NO+O2=2 NO2;③ |

(17分)下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体选择装置 (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置 。
(2)从碘水中分离出I2,选择装置 ,该分离方法的名称为 。
(3)装置A中①的名称是 ,进水的方向是 。
装置B在分液时为使液体顺利下滴,应进行的具体操作是
。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
 |
问题1:粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液; ②加入过量的BaCl2溶液; ③加入过量的NaOH溶液;
④调节溶液的pH等于7; ⑤溶解; ⑥过滤; ⑦蒸发。
正确的操作顺序是_____________(填写序号字母)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
问题2:按所选顺序操作时,步骤④的离子方程式是
。
问题3:由海水到氯化钠晶体的实验过程中要用到的主要装置是 (从给定的四种装置中选择)。



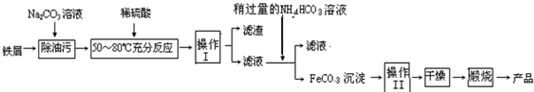
 (2010?天河区二模)铁及其化合物在日常生活应用广泛,请根据下列实验回答问题:
(2010?天河区二模)铁及其化合物在日常生活应用广泛,请根据下列实验回答问题:
 HCO3-+OH-
HCO3-+OH-
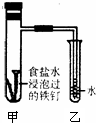 铁及其化合物在日常生活应用广泛,请根据下列实验回答问题:
铁及其化合物在日常生活应用广泛,请根据下列实验回答问题: