题目内容
某温度下,体积为1L的密闭容器中分别加入2molX、2molY、1molW、1molZ进行如下可逆反应:X(g)+Y(g) Z(s)+W(s);△H>0一段时间后反应达到平衡状态,下列叙述正确的是( )
Z(s)+W(s);△H>0一段时间后反应达到平衡状态,下列叙述正确的是( )
 Z(s)+W(s);△H>0一段时间后反应达到平衡状态,下列叙述正确的是( )
Z(s)+W(s);△H>0一段时间后反应达到平衡状态,下列叙述正确的是( )分析:A、固体量的增减不会引起化学平衡的移动;
B、从化学平衡的建立角度来分析;
C、当化学平衡的建立是逆向进行建立的,此时过程放热;
D、缩小容器的体积,相当于增大压强,则平衡向右进行,据此来回答.
B、从化学平衡的建立角度来分析;
C、当化学平衡的建立是逆向进行建立的,此时过程放热;
D、缩小容器的体积,相当于增大压强,则平衡向右进行,据此来回答.
解答:解:A、W在反应中是固体,固体量的增减不会引起化学平衡的移动和化学反应速率的改变,故A错误;
B、达到同一平衡时,可能是向正向进行建立的平衡,也可能是逆向进行建立的平衡,X和Z的浓度不可能都增大,故B错误;
C、如果上述反应在绝热系统中进行,化学平衡的建立是逆向进行建立的,此时过程放热,体系温度是升高的,故C错误;
D、缩小容器的体积,相当于增大压强,则平衡向右进行,气体的平均分子量=
,反应后气体质量减小,气体物质的量也减小,气体的平均分子量有可能增大,故D正确.
故选D.
B、达到同一平衡时,可能是向正向进行建立的平衡,也可能是逆向进行建立的平衡,X和Z的浓度不可能都增大,故B错误;
C、如果上述反应在绝热系统中进行,化学平衡的建立是逆向进行建立的,此时过程放热,体系温度是升高的,故C错误;
D、缩小容器的体积,相当于增大压强,则平衡向右进行,气体的平均分子量=
| m |
| n |
故选D.
点评:化学平衡的建立过程可以是正向进行建立的平衡,也可能是逆向进行建立的平衡,可以根据课本知识来解决,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
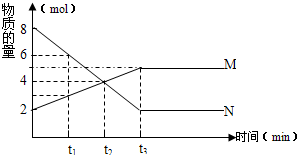 在一定温度下,容积为1L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,
在一定温度下,容积为1L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,
 Z(s)+W(s);△H>0一段时间后反应达到平衡状态,下列叙述正确的是( )
Z(s)+W(s);△H>0一段时间后反应达到平衡状态,下列叙述正确的是( )