题目内容
肼(N2H4)是一种可用于火箭或原电池的燃料.已知:
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ/mol ②
下列说法正确的是( )
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ/mol ②
下列说法正确的是( )
| A、反应①中反应物所具有的总能量大于生成物所具有的总能量 | B、2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-1000.3kJ/mol | C、铂做电极,KOH溶液做电解质溶液,由反应②设计的燃料电池其负极反应式:N2H4-4e-+4OH-=N2+4H2O | D、铂做电极,KOH溶液做电解质溶液,由反应②设计的燃料,工作一段时间后,KOH溶液的pH将增大 |
分析:A、反应①为吸热反应,反应后能量升高;
B、利用盖斯定律的计算,首先书写出化学方程式,在利用两个已知方程式推导出目标方程式,再求出反应热;
C、负极是N2H4失电子生成N2和H2O;
D、根据总方程分析溶液中氢氧根离子浓度的变化.
B、利用盖斯定律的计算,首先书写出化学方程式,在利用两个已知方程式推导出目标方程式,再求出反应热;
C、负极是N2H4失电子生成N2和H2O;
D、根据总方程分析溶液中氢氧根离子浓度的变化.
解答:解:A、已知N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol,该反应为吸热反应,反应后能量升高,所以反应物所具有的总能量小于生成物所具有的总能量,故A错误;
B、已知:N2(g)+2O2(g)═2NO2(g),△H=+67.7kJ/mol ①
N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-534kJ/mol ②
写出目标方程式为2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g),可以通过①②联立,2×②-①得到即2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g),△H=2×②-①=2×(-534kJ/mol)-(+67.7kJ/mol)=-1135.7kJ/mol,所以2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g),△H=-1135.7kJ/mol,故B错误;
C、负极是N2H4失电子生成N2和H2O,则其电极反应式为:N2H4-4e-+4OH-=N2+4H2O,故C正确;
D、已知该电池反应的总方程为:N2H4+O2=N2+2H2O,反应生成水,溶液的体积增大,所以氢氧化钾的浓度减小,即溶液的pH减小,故D错误;
故选C.
B、已知:N2(g)+2O2(g)═2NO2(g),△H=+67.7kJ/mol ①
N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-534kJ/mol ②
写出目标方程式为2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g),可以通过①②联立,2×②-①得到即2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g),△H=2×②-①=2×(-534kJ/mol)-(+67.7kJ/mol)=-1135.7kJ/mol,所以2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g),△H=-1135.7kJ/mol,故B错误;
C、负极是N2H4失电子生成N2和H2O,则其电极反应式为:N2H4-4e-+4OH-=N2+4H2O,故C正确;
D、已知该电池反应的总方程为:N2H4+O2=N2+2H2O,反应生成水,溶液的体积增大,所以氢氧化钾的浓度减小,即溶液的pH减小,故D错误;
故选C.
点评:本题考查了反应中能量变化,热化学方程式的书写方法和盖斯定律的计算应用,原电池原理的应用等,考查的内容较多,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
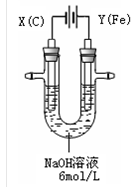
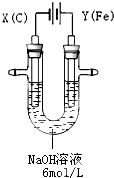 高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,成功率高,易于实验室制备.其原理如图所示.
高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,成功率高,易于实验室制备.其原理如图所示.
 Pb+PbO2+2H2SO4,则它在充电时的阳极反应为
Pb+PbO2+2H2SO4,则它在充电时的阳极反应为