题目内容
19.合成氨反应:N2(g)+3H2(g)?2ΝΗ3(g)△H=-92.4kJ•mol-1,在反应过程中,正反应速率的变化如图: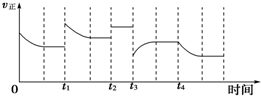
下列说法可能正确的是( )
| A. | t1时增大了压强 | B. | t2时增大了压强 | C. | t3时降低了温度 | D. | t4时降低了温度 |
分析 由图象可知,t1时正反应速率增大,t2时正逆反应速率同等程度增大,t3时正反应速率减小,t4时反应速率瞬间不变,然后减小,结合影响因素来解答.
解答 解:A、t1时正反应速率增大,且大于逆反应速率,则应为增大压强,故A正确;
B、t2时正逆反应速率同等程度增大,则为使用了催化剂,故B错误;
C、t3时正反应速率减小,且逆反应速率大于正反应速率,则为减小压强,故C错误;
D、t4时反应速率瞬间不变,然后减小,应为减小生成物浓度,故D错误;
故选A.
点评 本题考查影响化学反应速率的因素,注意把握浓度、催化剂、温度、压强对反应速率的影响即可解答,侧重反应速率图象的分析,明确速率变化程度为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
9.肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,反应生成N2和水蒸气.
已知:N2(g)+2O2(g)═N2O4(g);△H=+a kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g);△H=-b kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
已知:N2(g)+2O2(g)═N2O4(g);△H=+a kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g);△H=-b kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
| A. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-(b+a) kJ/mol | |
| B. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-(2b+a)kJ/mol | |
| C. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-(a-2b) kJ/mol | |
| D. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-(b-a) kJ/mol |
10.下列变化过程中,需要加入还原剂才能实现的是( )
| A. | Fe→FeSO4 | B. | SO2→S | C. | CO→CO2 | D. | HCl→Cl2 |
7.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 室温下体积为10L、pH=13的NaOH溶液中含有OH-的数目为NA | |
| B. | 常温常压下,17g氨气中含有氢原子的数目为NA | |
| C. | PH=1的醋酸溶液中,醋酸分子的个数为NA | |
| D. | 体积为1L、物质的量浓度为1mol•L-1的Na2CO3溶液中含有NA个CO32- |
4.分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法.从组成上分类,下列物质可以与CO2分为同一类的物质是( )
| A. | SO2 | B. | NaCl | C. | K2CO3 | D. | Al |
11.已知次氯酸是比碳酸还弱的酸,反应Cl2+H2O?HCl+HClO达到平衡后,要使HClO浓度增大,H+浓度减小,可加入( )
| A. | Na2SO3固体 | B. | 水 | C. | CaCO3固体 | D. | NaOH固体 |
8.下列关于化学反应速率的说法中,表述正确的是( )
| A. | 加入催化剂加快了反应速率,改变了反应吸收或放出的热量 | |
| B. | 对于某可逆反应,反应进行的净速率是正、逆反应速率之差 | |
| C. | 正反应速率越大,反应物的转化率越大 | |
| D. | 压强越大,活化分子百分数越大 |
9.H2有还原性,可以还原氧化铜,是因为H2中氢元素的化合价处于低价(0价),可以升高至+1价.由此分析:下列化学反应的反应物中的氢元素能体现还原性的是( )
| A. | Mg+2HCl═MgCl2+H2↑ | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | NaH+H2O═NaOH+H2↑ | D. | 2H2O2═2H2O+O2↑ |