题目内容
8.下列变化过程中,既有共价键断裂,又有离子键形成的是( )| A. | 溴化氢气体与氨气相遇反应 | B. | 氯化氢溶于水 | ||
| C. | 盐酸和NaOH溶液混合 | D. | 锌和稀硫酸反应 |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,有离子键和共价键断裂,说明变化为化学变化,以此来解答.
解答 解:A.发生化学变化生成氯化铵(离子化合物),H-Br共价键断裂,同时存在离子键形成,故A选;
B.只发生H-Cl的断裂,为电离过程,故B不选;
C.反应生成NaCl和水,在溶液中为氢离子与氢氧根离子结合生成水,不存在共价键断裂和离子键形成,故C不选;
D.反应生成硫酸锌和氢气,在溶液中为Zn与氢离子反应,不存在共价键断裂和离子键形成,故D不选;
故选A.
点评 本题考查化学键及化学变化,为高频考点,把握化学键的形成及判断、化学反应的实质为解答的关键,侧重分析与应用能力的考查,注意离子反应中化学键的变化,题目难度中等.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
18.常温下,下列叙述中不正确的是( )
| A. | NH4HSO4溶液中离子浓度大小关系:c(H+)>c(SO42-)>c(NH4+)>c(OH-) | |
| B. | 等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和,则a+b=14 | |
| C. | Na2C2O4溶液中:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) | |
| D. | NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
19.下列有关物质的性质与应用相对应的是( )
| A. | BaCO3能与盐酸反应,可用于治疗胃酸过多 | |
| B. | N2与O2在放电时生成NO,此反应用于工业制硝酸 | |
| C. | Al2O3熔点高,可用作耐高温材料 | |
| D. | 氢氟酸具有酸性,可用于雕刻玻璃 |
3.氢化锂(LiH)、氘化锂(LiD)、氘化锂(LiT)在一定条件下都可产生极高的能量,被广泛应用在火箭推进剂和核反应中.下列有关说法中,正确的是( )
| A. | LiH、LiD、LiT互为同素异形体 | |
| B. | LiH、LiD、LiT中氢元素的化合价均为+1 | |
| C. | H、D、T之间互称为同位素 | |
| D. | LiH、LiD、LiT在反应中常作氧化剂 |
13.下列离子方程式正确的是( )
| A. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 二氧化硫通入次氯酸钠溶液:SO2+ClO-+OH-=SO42-+Cl-+H2O | |
| C. | 硫酸工业尾气中的SO2用过量的氨水吸收:2NH3•H2O+SO2=2NH4++SO32-+H2O | |
| D. | Cu溶于浓HNO3:Cu+4H++2NO3-=Cu2++2NO↑+4H2O |
20.以海水为原料,不需经过化学变化就能获得的产品是( )
| A. | NaCl | B. | NaOH | C. | Mg | D. | Br2 |
17.下列分子中所有原子都满足最外层为8电子稳定结构的是( )
| A. | H2O2 | B. | CO2 | C. | PCl5 | D. | BF3 |
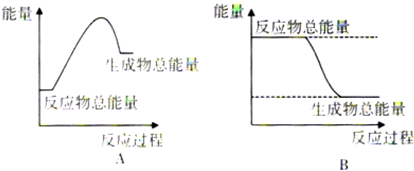
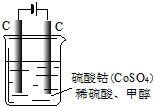 (1)甲醇可为燃料电池的原料.以CH4和H2O为原料,通过下列反应制备甲醇.
(1)甲醇可为燃料电池的原料.以CH4和H2O为原料,通过下列反应制备甲醇.