题目内容
【题目】大气中的臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:3O2![]() 2O3。
2O3。
(1)在臭氧发生器中装入100 mL O2,经反应3O2![]() 2O3,最后气体体积变为95 mL(体积均为标准状况下测定),则反应后混合气体的平均摩尔质量约为__________________密度为______ g·L-1。
2O3,最后气体体积变为95 mL(体积均为标准状况下测定),则反应后混合气体的平均摩尔质量约为__________________密度为______ g·L-1。
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为______ L。
【答案】 33.6g/mol 1.5 3
【解析】试题分析:(1)根据3O2![]() 2O3,利用差量法计算生成O3的体积,再根据
2O3,利用差量法计算生成O3的体积,再根据![]() 换算成物质的量;平均摩尔质量=
换算成物质的量;平均摩尔质量=![]() ;密度=
;密度=![]() ;(2)利用差量法计算生成O3的体积。
;(2)利用差量法计算生成O3的体积。
解析:(1)设生成O3的体积是 VmL;

V=10 mL,所以生成O3的体积是10 mL,剩余O2的体积是85 mL,根据![]() ;O3、O2的物质的量分别是
;O3、O2的物质的量分别是![]() 、
、![]() ,气体总质量是
,气体总质量是![]()
平均摩尔质量=![]() =
=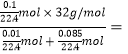 33.6g/mol ;密度=
33.6g/mol ;密度=![]() =
=![]() ;
;
(2)设生成O3的体积是VL

V=3L

练习册系列答案
相关题目