题目内容
10.下列金属中属于有色金属,且在常温下不溶于浓硝酸的是( )| A. | 铁 | B. | 镁 | C. | 铝 | D. | 铜 |
分析 铁、铬、锰属于黑色金属,其余的为有色金属,常温下铁、铝在浓硫酸、浓硝酸中发生钝化现象;
解答 解:铁、铬、锰属于黑色金属,其余的为有色金属,选项中镁、铝、铜为有色金属,常温下铁、铝在浓硫酸、浓硝酸中发生钝化现象,选项中Al符合属于有色金属,且在常温下不溶于浓硝酸,
故选C.
点评 本题考查了金属性质的分析应用主要是金属分类方法,金属的特征性质应用,主要是铁、铝在常温下在浓硫酸和浓硝酸中发生钝化,不能继续反应,题目较简单.

练习册系列答案
相关题目
20.对下列实验的描述不正确的是( )
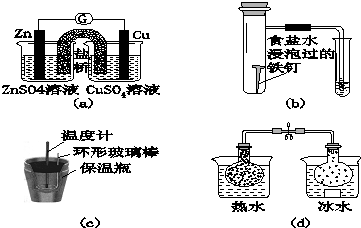

| A. | 图(a)所示的实验:根据检流计(G)中指针偏转的方向比较Zn、Cu的金属活泼性 | |
| B. | 图(b)所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀 | |
| C. | 图(c)所示的实验:根据温度计读数的变化用稀盐酸和稀NaOH溶液反应测定中和热 | |
| D. | 图(d)所示的实验:根据两烧瓶中气体颜色的变化判断2NO2(g)?N2O4(g)是放热反应 |
1.如图所示为气相直接水合法C2H4(g)+H2O(g)═C2H5OH(g)中乙烯的平衡转化率与温度、压强的关系[其中n(H2O):n(C2H4)=1:1].

计算乙烯水合制乙醇反应在图中A点的平衡常数Kp为 (用平衡分压代替平衡浓度计算,分压=总压物质的量分数)( )

计算乙烯水合制乙醇反应在图中A点的平衡常数Kp为 (用平衡分压代替平衡浓度计算,分压=总压物质的量分数)( )
| A. | 0.082 | B. | 0.072 | C. | 0.072MPa-1 | D. | 0.082 MPa-1 |
18.下列实验方案中,可行的是( )
| A. | 用氢氧化钠溶液除去CO2中的HCl气体 | |
| B. | 将白醋滴在湿润的pH试纸上,测定其pH | |
| C. | 按溶解、过滤、蒸发的操作顺序分离CaCl2、CaCO3的混合物 | |
| D. | 用BaCl2溶液除去KNO3溶液中少量的K2SO4 |
19.已知一种C(H+)=1×10-3mol•L-1的酸和一种C(OH-)=1×10-3mol•L-1的碱溶液等体积混合后溶液显碱性,其原因可能是( )
| A. | 浓的强酸和稀的强碱溶液反应 | |
| B. | 生成了一种强碱弱酸盐 | |
| C. | 浓的弱碱和稀的强酸溶液反应 | |
| D. | 等物质的量浓度的一元弱酸和一元强碱溶液反应 |
 氢化钙固体是登山运动员常用的能源提供剂.某兴趣小组拟选用如下装置制备氢化钙.已知CaH2+2H2O=Ca(OH)2+2H2↑;Ca+H2=CaH2.
氢化钙固体是登山运动员常用的能源提供剂.某兴趣小组拟选用如下装置制备氢化钙.已知CaH2+2H2O=Ca(OH)2+2H2↑;Ca+H2=CaH2. .
.