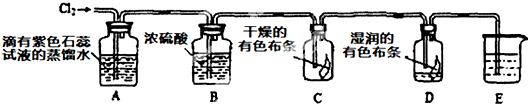
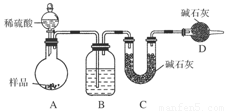
题目内容
化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中NaHCO3的质量分数。
[方案一]
称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为:
(2)实验中,需加热至恒重的目的是
。
[方案二]
称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。
(1)过滤操作中,除了玻璃棒、漏斗外,还要用到的玻璃仪器为 。
(2)实验中判断沉淀是否完全的方法是
。
[方案三]
按如下图所示装置进行实验: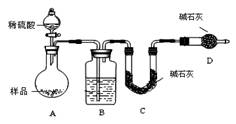
(1)D装置的作用是 。
分液漏斗中 (填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重 8.80g,则样品中NaHCO3的质量分数为 。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是:
。
[方案一]
(1)2NaHCO3△ Na2CO3 + CO2↑ + H2O(2)保证NaHCO3分解完全
[方案二]?
(1)烧杯?
(2)静置,往上层清液中继续滴加Ba(OH)2溶液,观察是否有白色沉淀生成
[方案三]?
(1)防止空气中的水蒸气、二氧化碳进入C装置 不能
(2)70.4%
(3)缺少一个驱赶残留二氧化碳气体的装置(或其他合理答案)
解析

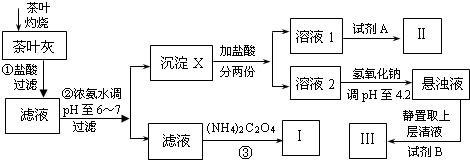
已知Ca2+、Al3+、Fe3+完全形成相应氢氧化物沉淀的pH如下表:
| Ca(OH)2 | Al(OH)3 | Fe(OH)3 | |
| pH | ≥13 | ≥5.2 | ≥4.1 |
(2)步骤②中调节pH至6~7的目的是
(3)沉淀X所含主要物质的化学式为
(4)写出步骤③中发生反应的离子方程式:
(5)试剂A为