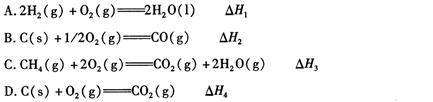题目内容
已知:
S(s)+O2(g) SO2(g) ΔH=-297.16 kJ·mol-1,
SO2(g) ΔH=-297.16 kJ·mol-1,
2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1。
2SO3(g) ΔH=-196.6 kJ·mol-1。
下列说法正确的是 ( )
S(s)+O2(g)
 SO2(g) ΔH=-297.16 kJ·mol-1,
SO2(g) ΔH=-297.16 kJ·mol-1,2SO2(g)+O2(g)
 2SO3(g) ΔH=-196.6 kJ·mol-1。
2SO3(g) ΔH=-196.6 kJ·mol-1。下列说法正确的是 ( )
| A.1 mol SO2(g)的能量总和大于1 mol S(s)和1 mol O2(g)的能量总和 |
| B.将2 mol SO2(g)与1 mol O2(g)在一定条件下充分反应,放出196.6 kJ的热量 |
| C.S(g)+O2(g)=SO2(g) ΔH=-Q,Q值小于297.16 kJ |
| D.当1 mol S(s)完全转化为SO3(g)时(假设无热量损失),放出395.46 kJ的热量 |
D
放热反应生成物的能量总和小于反应物的能量总和,A项错误;B项忽视了可逆反应不能进行彻底,错误;气态硫燃烧放出的热量比液态硫燃烧放出的热量多,C项错误;根据盖斯定律,第一个方程式+第二个方程式× 可得S(s)+
可得S(s)+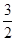 O2(g)=SO3(g) ΔH=-395.46 kJ·mol-1,D项正确
O2(g)=SO3(g) ΔH=-395.46 kJ·mol-1,D项正确
 可得S(s)+
可得S(s)+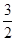 O2(g)=SO3(g) ΔH=-395.46 kJ·mol-1,D项正确
O2(g)=SO3(g) ΔH=-395.46 kJ·mol-1,D项正确
练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
 ,该分子中有________个σ键,________个π键,有________种极性键,________(填“有”或“没有”)非极性键。
,该分子中有________个σ键,________个π键,有________种极性键,________(填“有”或“没有”)非极性键。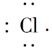

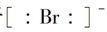
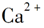
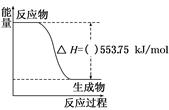
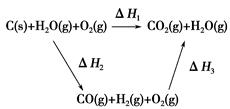
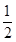 O2(g)=CO(g)的ΔH。但可设计实验、利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有________。
O2(g)=CO(g)的ΔH。但可设计实验、利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有________。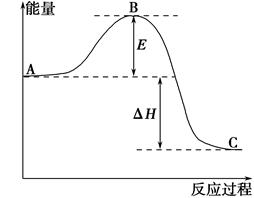
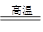 CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为: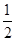 O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1