题目内容
【题目】图为一原电池装置,下列叙述中正确的是
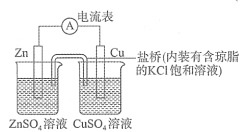
A.该装置中电子由Zn电极流向Cu电极,溶液中的![]() 通过盐桥移向Zn极
通过盐桥移向Zn极
B.将上述装置中的Zn棒和Cu棒同时浸入CuSO4溶液,电流表的指针偏转幅度变小,且很快减弱
C.将烧杯内溶液对换,电流表指针发生偏转
D.将盐桥改为铜导线连接两种溶液,电流由Cu电极移向Zn电极
【答案】B
【解析】Zn作负极,Cu作正极,在外电路中电子由Zn电极流向Cu电极,在内电路的盐桥中Cl移向ZnSO4溶液,K+移向CuSO4溶液,A错误;若将Zn棒和Cu棒同时浸入CuSO4溶液,也构成原电池,产生电流,但效率不高,电流会很快衰减,B正确;若将溶液对换,则Zn直接将Cu置换出来附着在Zn表面,不能形成电流,C错误;因Cu导线不能传递离子,用其替换盐桥不能构成闭合电路,不产生电流,D错误。

练习册系列答案
相关题目
【题目】由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是______________________________________。
(2)装置乙中正极的电极反应式是_______________________________________。
(3)装置丙中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)四种金属活动性由强到弱的顺序是___________________________________。