题目内容
硫酸是重要的化工材料,二氧化硫生成三氧化硫是工业制硫酸的重要反应之一。
(1)将0.050 mol SO2(g)和0.030 mol O2(g)放入容积为1 L的密闭容器中,反应
2SO2(g)+O2(g)![]() 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。
① 从平衡角度分析采用过量O2的目的是 ;
② 计算该条件下反应的平衡常数K=___________。ks5u
③ 已知:K(300℃)>K(350℃),该反应是________热反应。若反应温度升高,SO2的转化率 (填“增大”、“减小”或“不变”)。
(2)某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图1所示。平衡状态由A变到B时,平衡常数K(A)_______K(B)(填“>”、“<”或“=”,下同)。
(3)如图2所示,保持温度不变,将2 mol SO2和1 mol O2加入甲容器中,将4 mol SO3加入乙容器中,隔板K不能移动。此时控制活塞P,使乙的容积为甲的2倍。
①若移动活塞P,使乙的容积和甲相等,达到新平衡时,SO3的体积分数甲 乙。
②若保持乙中压强不变,向甲、乙容器中通入等质量的氦气,达到新平衡时,SO3的体积分数甲 乙。(在① 、②填入:大于、等于、小于)
、②填入:大于、等于、小于)

(1)①提高二氧化硫的转化率;②1600;③放热;减小
(2)=
(3)①<;②>

练习册系列答案
相关题目
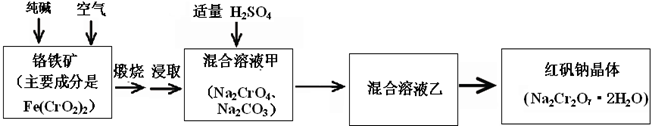

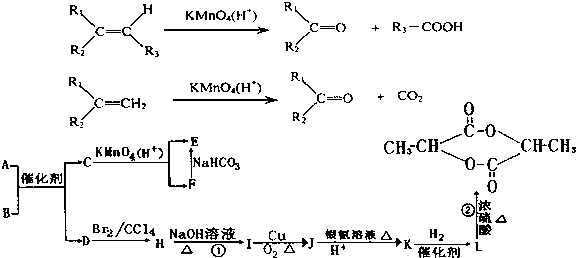

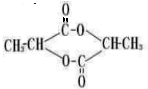 +2H2O
+2H2O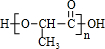 +(n-1)H2O
+(n-1)H2O




 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。 