题目内容
5.反应Cu+HNO3→Cu(NO3)2+NO+H2O中,9.6g Cu消耗做氧化剂的HNO3( )| A. | 0.4mol | B. | 0.3mol | C. | 0.2mol | D. | 0.1mol |
分析 氧化还原反应中一定遵循电子守恒,根据n=$\frac{m}{M}$计算出9.6g铜的物质的量,从而得出铜完全反应生成电子的物质的量;反应中做氧化剂的硝酸被还原生成NO气体,根据电子守恒可知被做氧化剂还原的硝酸的物质的量即可.
解答 解:9.6g铜的物质的量为:$\frac{9.6g}{64g/mol}$=0.15mol,0.15mol铜完全反应生成铜离子失去0.3mol电子,
反应中做氧化剂的硝酸被还原生成NO气体,根据电子守恒可知被做氧化剂还原的硝酸的物质的量为:$\frac{0.3mol}{5-2}$=0.1mol,
故选D.
点评 本题考查了氧化还原反应的计算,题目难度不大,明确氧化还原反应中电子守恒的含义为解答关键,注意掌握氧化还原反应的实质及特征,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
19.医学家最近合成了一种具有抗癌活性的化合物Depudecin,该物质也曾从真菌里分离出来,其结构简式如下: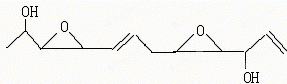
下列关于该化合物的说法正确的是( )

下列关于该化合物的说法正确的是( )
| A. | 该化合物的分子式为C12H16O4 | |
| B. | 该化合物属于有机酯类,所以可以发生水解反应 | |
| C. | 该化合物既可以发生消去反应,也可以被催化氧化生成醛 | |
| D. | 1mol该化合物可以和2mol醋酸发生取代反应 |
16.可逆反应aA(s)+bB(g)?cC(g)+dD(g),当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,据图分析,以下正确的是( )

| A. | P1>P2,a+b=c+d | B. | Pl<P2,b=c+d | ||
| C. | T1>T2,正反应放热 | D. | Tl<T2,正反应吸热 |
17.研究CO2的利用对促进低碳社会的构建具有重要的意义.
(1)在一定体积的密闭容器中,进行化学反应:CO2(g)+H2(g)?CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如表:
①该反应正向反应是吸热反应.(填“放热”或“吸热”)
②能判断该反应达到化学平衡状态的依据是BC.
A.容器压强不变 B.混合气体中c(CO2)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
③当其他条件不变时,若缩小容器的体积,该反应平衡不移动.(选填“正向”、“逆向”或“不”)
(2)工业上合成甲醇可在密闭容器中采用如下反应进行:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
①该反应的平衡常数表达式K=$\frac{c(CH{\;}_{3}OH)c(H{\;}_{2}O)}{c(CO{\;}_{2})c{\;}^{3}(H{\;}_{2})}$.
②某实验将1molCO2和3molH2充入一定体积的密闭容器中,在两种不同条件下发生反应(只有一种条件不同).测得CH3OH的物质的量随时间变化如图所示:
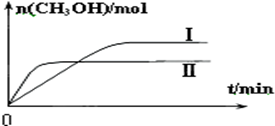
曲线I、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(选填“>”、“=”或“<”).
③一定温度下,在容积2L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
经测定甲容器经过5min达到平衡,平衡时CO2的转化率为50%,甲容器中该反应在5min内的平均速率υ(H2)=0.15mol•L-1•min-1.
要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为0.5<n(c)<1.
(1)在一定体积的密闭容器中,进行化学反应:CO2(g)+H2(g)?CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如表:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
②能判断该反应达到化学平衡状态的依据是BC.
A.容器压强不变 B.混合气体中c(CO2)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
③当其他条件不变时,若缩小容器的体积,该反应平衡不移动.(选填“正向”、“逆向”或“不”)
(2)工业上合成甲醇可在密闭容器中采用如下反应进行:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
①该反应的平衡常数表达式K=$\frac{c(CH{\;}_{3}OH)c(H{\;}_{2}O)}{c(CO{\;}_{2})c{\;}^{3}(H{\;}_{2})}$.
②某实验将1molCO2和3molH2充入一定体积的密闭容器中,在两种不同条件下发生反应(只有一种条件不同).测得CH3OH的物质的量随时间变化如图所示:

曲线I、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(选填“>”、“=”或“<”).
③一定温度下,在容积2L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为0.5<n(c)<1.
15.下列各组物质中,互为同分异构体的是( )
| A. | 12C和14C | B. | O2和O3 | ||
| C. | CH2=CHCH3和CH3CH=CHCH3 | D. | CH3CH2C≡CH和CH2=CHCH=CH2 |
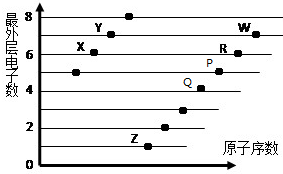 如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系.
如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系.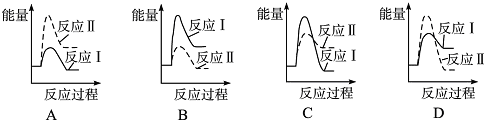
 碳、氮及其化合物在工农业生产生活中有着重要作用.请回答下列问题:
碳、氮及其化合物在工农业生产生活中有着重要作用.请回答下列问题: