题目内容
18.下列实验中,所选取的分离装置与对应原理都正确的是( )| 选项 | 目的 | 装置 | 原理 |
| A | 氢氧化铁胶体的纯化 | ① | 胶体粒子不能通过滤纸,离子及小分子可以通过滤纸 |
| B | 分离苯中的溴苯 | ③ | 苯(0.88g/mL)和溴苯(1.5g/mL)的密度不同 |
| C | 粗盐提纯 | ② | NaCl在水中的溶解度很大 |
| D | 除去环己醇中的环己烯 | ④ | 环己醇的沸点(161℃)与环己烯的沸点(83℃)相差较大 |

| A. | A | B. | B | C. | C | D. | D |
分析 A.胶体粒子可透过滤纸;
B.苯和溴苯混溶;
C.粗盐的提纯用蒸发的方法,与沸点有关;
D.混合物的沸点不同,可蒸馏分离.
解答 解:A.胶体粒子可透过滤纸,不能用过滤的方法,应用渗析的方法分离,故A错误;
B.苯和溴苯混溶,应用蒸馏的方法分离,故B错误;
C.粗盐的提纯用蒸发的方法,与溶解度无关,利用了水易挥发的特点,与沸点有关,故C错误;
D.环己醇、环己烯混合物的沸点不同,可蒸馏分离,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的分离与提纯等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
相关题目
17.己知A、B、C、D为短周期元素组成的四种物质,且D为强电解质.在一定条件下有如下转化关系:A$\stackrel{O_{2}}{→}$B$\stackrel{O_{2}}{→}$C$\stackrel{H_{2}O}{→}$D(其他相关物质可能省略).下列说法不正确的是( )
| A. | A不可能为碳单质 | |
| B. | 若A为金属单质,则 A-定位于第三周期第IA族 | |
| C. | 若常温下D的浓溶液能使铁、铝钝化,则A可能是单质,也可能是化合物 | |
| D. | 若A是共价化合物,A的水溶液一定显碱性 |
6.下列图示实验操作,能达到目的是( )
| A. |  检验K+的存在 检验K+的存在 | B. | 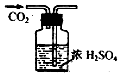 干燥CO2 | C. |  分离酒精与水 分离酒精与水 | D. |  蒸发食盐水 |
3.下列离子方程式书写正确的是( )
| A. | Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+H2O | |
| B. | NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 过量SO2通入到NaClO溶液中:SO2+H2O+ClO-═HClO+HSO3- | |
| D. | NaAlO2溶液和过量的HCl溶液反应:AlO2-+H++H2O═Al(OH)3↓ |
10.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1,则氢气的燃烧热为241.8 kJ•mol-1 | |
| B. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量 | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,则石墨比金刚石稳定 | |
| D. | 己知2C(s)+2O2(g)═2CO2(g)△H=a kJ•mol-1,2C(s)+O2(g)═2CO(g)△H=b kJ•mol-1,则a>b |
8.下表列出了A~R九种元素在元素周期表中的位置:
(1)这九种元素分别为ANa、BK、CMg、DAl、EN、FO、GS、HCl、RAr,其中化学性质最不活泼的是Ar.
(2)A、B、C三种元素按原子半径由大到小的顺序排列为K>Na>Mg(用元素符号表示).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | H | R | ||
| 4 | B |
(2)A、B、C三种元素按原子半径由大到小的顺序排列为K>Na>Mg(用元素符号表示).

 ;
; ;
;
 .
. .
.