题目内容
【题目】在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,X和Y两物质的浓度随时间变化情况如图。

(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):_________________________。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是________________。
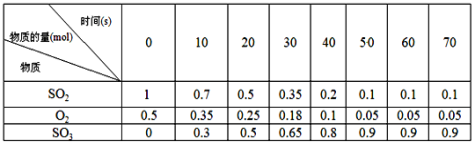
素材1:某温度和压强下,2L容器中,发生反应2SO2+O2![]() 2SO3,不同时间点测得密闭体系中三种物质的物质的量如下:
2SO3,不同时间点测得密闭体系中三种物质的物质的量如下:
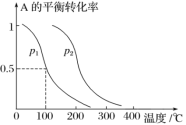
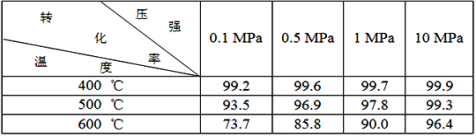
素材2:反应在不同条件下进行时SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的百分数,SO2的转化率越大,化学反应的限度越大)
根据以上的两个素材回答问题:
(3)根据素材1中计算20~30s期间,用二氧化硫表示的化学反应平均速率为________。
(4)根据素材2中分析得到,提高该化学反应限度的途径有_______________。
(5)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应具体条件是__________________。
【答案】Y![]() 2X bd 0.0075mol·L-1·s-1 增大压强或(在一定范围内或适当)降低温度 温度为600℃,压强为1MPa
2X bd 0.0075mol·L-1·s-1 增大压强或(在一定范围内或适当)降低温度 温度为600℃,压强为1MPa
【解析】
结合反应物和生成物的浓度变化量与化学计量数成正比解题;根据平衡状态的特征分析;利用速率公式、转化率公式计算。
(1)由图可知,X的物质的量增加,Y的物质的量减少,则X为生成物,Y为反应物,由10mim达到平衡可知,Y、X的浓度变化量之比为(0.6-0.4)mol/L:(0.6-0.2)mol/L=1:2,则反应方程式为:Y2X;
(2)由图可知,10-25min及35min之后X、Y的物质的量不发生变化,则相应时间段内的点处于化学平衡状态,即b、d处于化学平衡状态,故答案为:b、d;
(3)由素材1可知,20-30s内二氧化硫的物质的量的变化量为0.5mol-0.35mol=0.15mol,
则二氧化硫表示的化学反应的平均速率为 =0.0075 molL-1s-1;
=0.0075 molL-1s-1;
(4)由素材2可知,压强越大、温度越低时有利于提高该化学反应限度,但温度太低时反应速率较慢,则提高该化学反应限度的途径有增大压强或在一定范围内降低温度;
(5)由素材1可知,50s时反应达到平衡,则二氧化硫的转化率为![]() =90%,结合素材2可知,转化率为90%时温度为600℃,压强为1MPa。
=90%,结合素材2可知,转化率为90%时温度为600℃,压强为1MPa。

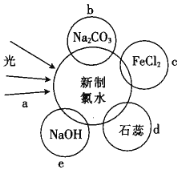
【题目】A、B、C、D四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
阴离子 | Cl-、SiO32-、OH-、NO3- |
阳离子 | H+、Ag+、Na+、K+ |
已知:A溶液呈强酸性,且A溶液与B、C溶液混合均产生白色沉淀,B的焰色反应呈黄色。
回答下列问题:
(1)写出A、B、C、D的化学式:A______,B_____,C____,D____。
(2)写出A溶液与B溶液反应的离子方程式: __________。
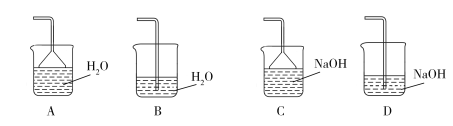
(3)请选出适合存放A、C、D溶液的试剂瓶的序号:
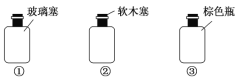
溶液 | A | C | D |
试剂瓶序号 | ___ | ___ | ___ |