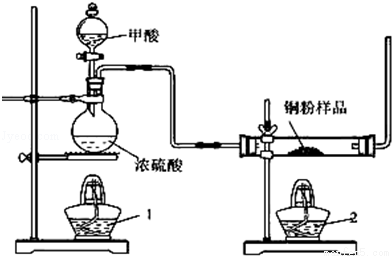
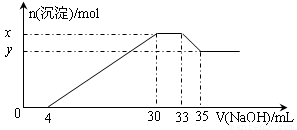
题目内容
下列各种说法中,正确的是 ( )
A.3号到9号元素化合价的变化与11到17号元素化合价的变化完全相同
B.同周期原子半径逐渐减小,所以离子半径也逐渐减小
C.随着原子序数的递增,碱金属元素单质的还原性逐渐增强,阳离子的氧化性逐渐减弱
D.甲乙电子层数相同,甲的最高价氢氧化物的碱性比乙的最高价氢氧化物的碱性强,说明甲的核电荷数比乙大
C
【解析】
试题分析:A.与11到17号元素化合价的变化规律基本重复3号到9号元素化合价的变化。但是8号元素O、9号元素F无正价,而16号元素S、17号元素Cl则有+6、+7价。错误。B.同周期原子半径逐渐减小,但是同一周期的金属元素形成的离子是上一周期是惰性气体的原子结构;同一周期的非金属元素形成的阴离子为同一周期是该周期的惰性气体的原子结构。比该周期的计算元素的离子多一个电子层。半径比金属离子的大。对于对称层结构相同的微粒来说,核电荷数越大,离子半径越小;对于电子层结构不同的微粒来说,电子层数越多,离子半径越大。错误。C.同一主族的元素,从上到下,随着原子序数的递增,原子半径逐渐增大,碱金属元素单质的还原性逐渐增强,阳离子的氧化性逐渐减弱。正确。D.甲乙电子层数相同,甲的最高价氢氧化物的碱性比乙的最高价氢氧化物的碱性强,说明甲的核电荷数比乙小。错误。
考点:考查元素周期表、元素周期律的应用的知识。

现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第3周期元素的简单离子中半径最小 |
(1)画出元素T的原子结构示意图__________________________;
(2)元素Y与元素Z相比,金属性较强的是__________________(用元素符号表示),下列表述中能证明这一事实的是_________________(填序号);
a.Y单质的熔点比Z单质低b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式___________,并写出该化合物与水反应的离子方程式______;
(4)元素T和氢元素以原子个数比1∶1化合形成的化合物属于______________,元素Z与元素T形成的化合物属于____________________(以上两空选填“共价化合物”或“离子化合物”)。