题目内容
【题目】在溶液中,反应![]()
![]() C分别在三种不同实验条件下进行,它们的起始状态均为:
C分别在三种不同实验条件下进行,它们的起始状态均为: ![]() 、
、![]() 、
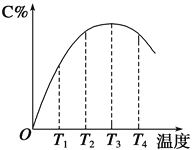
、![]() 。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是( )
。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是( )

A. 反应的平衡常数:①<②
B. 反应A+2B![]() C的
C的![]()
C. 实验②平衡时B的转化率为60%
D. 实验③平衡时![]()
【答案】B
【解析】①、②平衡时浓度不变,反应的平衡常数不变,到达平衡的时间不同,说明速率不同,A错误;由①、③平衡时浓度比较,③平衡时浓度小于①平衡时浓度,且达到平衡时间短,又因此反应在溶液中进行,可能的条件是升高温度,平衡正向移动,则正反应吸热反应,B正确;实验③中A物质的浓度变化量为![]() ,实验③平衡时
,实验③平衡时![]() A物质的浓度变化量=
A物质的浓度变化量=![]() ,D错误;实验②平衡时B
,D错误;实验②平衡时B
的转化浓度为A的转化浓度的2倍,即![]() ,则B的转化率为
,则B的转化率为![]() /
/![]() =40%,B错误。(可以由三段式解题)。
=40%,B错误。(可以由三段式解题)。

 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案【题目】某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、H+、SO42﹣、CO32﹣ .
(1)为了进一步确认,对该溶液进行实验检测:
实验操作与现象 | 实验结论 | 判断理由 | |
步骤一 | 仔细观察坐标图 | 肯定无 | 肯定无该离子的理由 |
步骤二 | 该溶液呈无色、透明、均一状态 | 肯定无 | 肯定无该离子的理由 |
步骤三 | 加入足量BaCl2溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失 | 肯定有SO42﹣、H+;肯定无Ba2+ | 肯定有H+的理由 |
实验操作的步骤三中称量沉淀前的实验操作步骤有:过滤、、灼烧、在干燥器中冷却.
(2)原溶液中H+物质的量浓度为mol/L.
(3)向溶液中加入NaHCO3溶液,反应的离子方程式为: .
(4)若向 100mL 该溶液中加入 1mol/L 的 Ba(OH)2溶液,恰好沉淀完全时加入的Ba(OH)2溶液体积为 L. 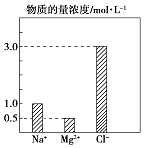
【题目】只给出下列甲中和乙中对应的量,不能组成一个求物质的量的公式的是( )
甲 | 乙 | |
① | 物质微粒数 | 阿伏加德罗常数 |
② | 标准状况下气体摩尔体积 | 标准状况下气体体积 |
③ | 固体体积 | 固体密度 |
④ | 溶液中溶质的质量分数 | 溶液的体积 |
⑤ | 非标准状况下物质的质量 | 物质的摩尔质量 |
A.③
B.③④
C.②③④
D.③④⑤