题目内容
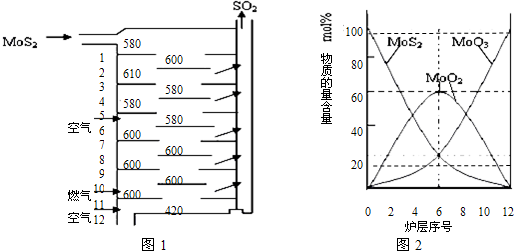
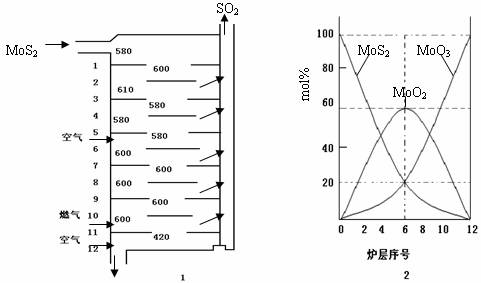
辉钼矿(MoS2)是钼最重要的矿物。图1是辉钼矿多层焙烧炉的示意图,其中1,2,3,…是炉层编号。580,600,610,…是各炉层的温度(℃)。图2给出了各炉层的固体物料的摩尔百分组成。
已知:MoS2焙烧生成1molMoO3的反应热为ΔH1=-1011KJ/mol,MoO2氧化生成1molMoO3的反应热为ΔH2=-154KJ/mol。试回答:
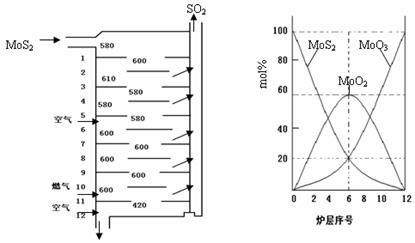
图1 图2
(1)辉钼矿焙烧生成MoO3的反应中被氧化的元素是: ;指出辉钼矿焙烧生成的尾气对环境的一种危害: 。
(2)第6炉层存在的固体物质分别是: ;它们的物质的量之比是: 。
(3)辉钼矿焙烧生成MoO3的热化学反应方程式是: 。
(4)图26―2表明,中间炉层(4~6)可能存在一种“固体+固体→固体+…”的反应,请写出该反应的化学方程式: 。
(5)通过(3)和(4)你能解释为什么中间炉层(4~6)的炉温比上下炉层的炉温低吗? 。
【解析】该题主要考查学生识图能力、阅读理解能力和运用化学知识的能力。
【答案】(1)Mo和S;形成酸雨
(2)MoS2、MoO3、MoO2;1:1:3。
(3)MoS2 (s)+ 3.5O2 (g)= MoO3(s) + 2SO2(g) ΔH1=-1011KJ/mol.
(4)MoS2 + 6MoO3 = 7MoO2 + 2SO2
(5)由① MoS2 (s)+ 3.5O2 (g)= MoO3(s) + 2SO2(g) ΔH1=-1011KJ/mol和
② MoO2(s)+ 0.5O2 (g)= MoO3(s) ΔH2=-154KJ/mol
得反应③MoS2 (s)+ 6MoO3 (s)= 7MoO2 (s)+ 2SO2(g)
△ H3=ΔH1-7ΔH2=-1011KJ/mol-(-154KJ/mol)×7=67KJ/mol,因为ΔH3>0,
故反应③是吸热反应,因其发生在中间层,故炉温降低。