题目内容
(每空2分,共10分)(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是_____
A、KMnO4 B、 H2O2 C、 Cl2水 D、 HNO3
然后再继续加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+
而不损失CuSO4的目的,调整溶液pH可选用下列中的________
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)向25 mL氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,得到曲线如下图所示
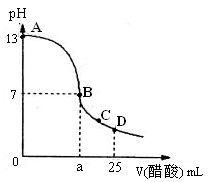
①、写出氢氧化钠溶液与醋酸溶液反应的离子方程式
②、该氢氧化钠溶液的物质的量浓度为
③、在B点,a 12.5 mL(填“大于”、“小于”或“等于”)
A、KMnO4 B、 H2O2 C、 Cl2水 D、 HNO3
然后再继续加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+
而不损失CuSO4的目的,调整溶液pH可选用下列中的________
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)向25 mL氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,得到曲线如下图所示

①、写出氢氧化钠溶液与醋酸溶液反应的离子方程式
②、该氢氧化钠溶液的物质的量浓度为
③、在B点,a 12.5 mL(填“大于”、“小于”或“等于”)
(1)B CD (2)①CH3COOH+OH—=CH3COO— + H2O ②0.1 mol·L—1 ③大于
(1)除杂时不能再引入新的杂质,ACD均会引入新的杂质,双氧水的还原产物是水,没有杂质,所以答案是B。同样调整溶液pH时也不能引入新的杂质,所以选项CD正确。
(2)滴定前氢氧化钠的pH是13,所以浓度是0.1mol/L。醋酸是弱酸,当二者恰好反应时,溶液显碱性,B的显中性,说明醋酸的体积大于12.5 mL。
(2)滴定前氢氧化钠的pH是13,所以浓度是0.1mol/L。醋酸是弱酸,当二者恰好反应时,溶液显碱性,B的显中性,说明醋酸的体积大于12.5 mL。

练习册系列答案
相关题目
 四种溶液分别盛于A、B、C、D四支试管中,进行如下实验:① A、B混合产生蓝色沉淀;②将A、D混合产生白色沉淀;
四种溶液分别盛于A、B、C、D四支试管中,进行如下实验:① A、B混合产生蓝色沉淀;②将A、D混合产生白色沉淀;