题目内容
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJmol﹣1表示.请认真观察如图,然后回答问题. 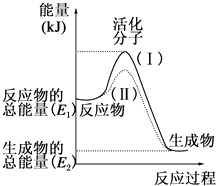
(1)图中所示反应是(填“吸热”或“放热”)反应.
(2)已知拆开1mol H﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ.则由1mol氢气和1mol 碘反应生成HI会(填“放出”或“吸收”)kJ的热量.在化学反应过程中,是将转化为 .
(3)下列反应中,属于放热反应的是 , 属于吸热反应的是 .
①物质燃烧
②炸药爆炸
③酸碱中和反应
④二氧化碳通过炽热的碳
⑤食物因氧化而腐败
⑥Ba(OH)28H2O与NH4Cl反应
⑦铁粉与稀盐酸反应.
【答案】
(1)放热
(2)放出;11;化学能;热能
(3)①②③⑤⑦;④⑥
【解析】解:(1)依据图象分析反应物的能量大于生成物的能量,反应放热,所以答案是:放热;(2)在反应H2+I22HI中,断裂1molH﹣H键,1molI﹣I键共吸收的能量为:1×436kJ+151kJ=587kJ,生成2molHI,共形成2molH﹣I键,放出的能量为:2×299kJ=598kJ,吸收的能量少,放出的能量多,所以该反应为放热反应,放出的热量为:598kJ﹣587kJ=11kJ所以答案是:放出;11;(3)①物质燃烧属于放热反应; ②炸药爆炸属于放热反应; ③酸碱中和反应属于放热反应; ④二氧化碳通过炽热的碳虽然属于化合反应,但为吸热反应;⑤食物因氧化而腐败属于放热反应; ⑥Ba(OH)28H2O与NH4Cl反应为吸热反应 ⑦铁粉与稀盐酸反应属于放热反应;所以放热反应有:①②③⑤⑦;吸热反应有:④⑥,所以答案是:①②③⑤⑦;④⑥.
【考点精析】利用吸热反应和放热反应对题目进行判断即可得到答案,需要熟知化学上把吸收热量的化学反应称为吸热反应;化学上把放出热量的化学反应称为放热反应.

 名校课堂系列答案
名校课堂系列答案【题目】在T ℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸(T ℃),测得混合溶液的部分pH如下表所示:
序号 | 氢氧化钠溶液的体积 | 盐酸的体积 | 溶液的pH |
① | 20.00 | 0.00 | 10 |
② | 20.00 | 20.00 | 6 |
假设溶液混合前后的体积变化忽略不计,则c为( )
A. 1 B. 4 C. 2 D. 6
