题目内容
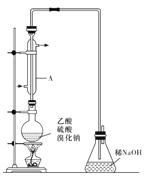
【题目】某研究小组模拟工业处理电镀含氰废水并测定处理的效率,利用下图所示装置进行实验。将CN-的浓度为0.2 mol·L-1的含氰废水100 mL与100 mL NaClO溶液(过量)置于装置②三颈烧瓶中,充分反应。打开分液漏斗活塞,滴入100 mL稀H2SO4,关闭活塞。

已知装置②中发生的主要反应依次为:
CN-+ ClO-=CNO-+ Cl- 2CNO-+2H+ +3C1O-=N2↑+2CO2↑+3C1-+H2O
(1)①和⑥的作用是 。
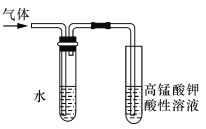
(2)装置②中,生成需由装置③除去的物质的离子方程式为 。
(3)反应结束后,缓缓通入空气的目的是 。
(4)为计算该实验中含氰废水被处理的百分率,需要测定 的质量。
(5)已知CN-的处理效率可高达90%,产生的CO2在标准状况下的体积为 。(保留一位小数)
【答案】(1)排除空气中CO2对实验的干扰;
(2)ClO-+Cl-+2H+=Cl2↑+H2O;
(3)使装置内残留的CO2全部进入装置⑤而被吸收;
(4)装置⑤反应前后的质量或沉淀;(5)0.4L。
【解析】
试题分析:(1)实验的原理是利用CN-+ ClO-=CNO-+ Cl- ;2CNO-+2H+ +3C1O-=N2↑+2CO2↑+3C1-+H2O,通过测定碱石灰的质量的变化测得二氧化碳的质量,根据关系式计算含氰废水处理百分率,实验中应排除空气中二氧化碳的干扰,防止对装置⑤实验数据的测定产生干扰,所以装置①和⑥的作用是排除空气中CO2对实验的干扰。
(2)根据已知装置②中发生的主要反应依次为CN-+ ClO-=CNO-+ Cl- ;2CNO-+2H+ +3C1O-=N2↑+ 2CO2↑+3C1-+H2O,,可知溶液中有氯离子、氢离子和次氯酸根离子,酸性条件下,氯离子和次氯酸根离子反应生成氯气,产生的氯气用碘化钾吸收,所以发生反应的离子方程式为ClO-+Cl-+2H+=Cl2↑+H2O;
(3)反应后装置中残留二氧化碳,应继续缓缓通入净化的空气,将装置内的残留的二氧化碳全部进入装置⑤,以减少实验误差,所以反应结束后,缓缓通入空气的目的是使装置中残留的二氧化碳全部进入装置⑤而被吸收。
(4)通过测定氢氧化钡溶液的质量的变化测得二氧化碳的质量,根据关系式计算含氰废水处理百分率,则需要测定装置⑤反应前后的质量或沉淀;
(5)根据碳元素守恒可知被处理的CN﹣的物质的量为n(CN﹣)=n(CO2)=0.02mol×90%=0.018mol,所以标准状况下的体积为0.018mol×22.4L/mol=0.4L,

 名校课堂系列答案
名校课堂系列答案